
前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)C的元素符号为 D2+的电子排布式为_______。
(2)四种元素中第一电离最小的是________,电负性最大的是________。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
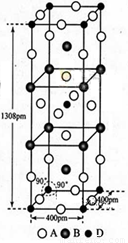
该化合物的化学式为_________;D的配位数为_______;该晶体的密度为_______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_____;该化合物中存在一个复杂离子,该离子的化学式为_______,配位体是____。
(1)Fe 1s22s22p63s23p63d8 (2)K F
(3)①K2NiF4 6 ② 3.4 (4)离子键和配位键 FeF63- F-
【解析】
试题分析:A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8。又因为A的原子序数小于B的原子序数,则A应该是F,B是K;K是第四周期,元素,与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2,实验根据C的原子序数小于D的可知,C是Fe,D是Ni。
(1)根据构造原理可知,D2+的电子排布式为1s22s22p63s23p63d8。
(2)金属性越强,第一电离能越小,非金属越大,电负性越大,所以四种元素中第一电离最小的是K,电负性最大的是F。
(3)①根据晶胞的结构简式可知,F原子的个数是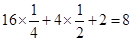 ;K原子的个数是
;K原子的个数是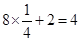 ;Ni原子个数是
;Ni原子个数是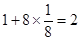 ,所以该化合物的化学式是K2NiF4。
,所以该化合物的化学式是K2NiF4。
②根据晶胞的结构简式可知,中间的立方体中Ni原子周围最近的F原子个数是6,既配位数是6。
③根据①可知该晶胞的目的应该是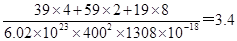 g·cm-3。
g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物是K3[FeF6],含有的化学键是离子键和配位健,其中复杂的离子是[FeF6]3-,配体是F-。
考点:考查核外电子排布式、第一电离能、电负性、化学键、配位健以及晶体类型的有关计算和判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源: 题型:阅读理解
 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:



查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)依据第2周期元素第一电离能的变化规律,参照如图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.
(1)依据第2周期元素第一电离能的变化规律,参照如图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅱ卷带解析) 题型:填空题
[化学—选修3:物质结构与性质](15分)
前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,平且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为_______。
(2)四种元素中第一电离最小的是________,电负性最大的是________。(填元素符号)
(3)A、B和D三种元素责成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________________;D的配位数为___________;
②列式计算该晶体的密度_______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_____________;该化合物中存在一个复杂离子,该离子的化学式为_______________,配位体是____________。
查看答案和解析>>
科目:高中化学 来源:2014届河南省许昌平顶山新乡三市高三第一次调研理综化学试卷(解析版) 题型:填空题
前四周期原子序数依次增大的元素A,B,C,D中, A是电负性最大的元素,并且A-和B+的电子数相差为8;C和D原子序数相差为2,且都与B位于同一周期,C元素的次外层电子数是最外层电子数的7倍。

回答下列问题:
(1)D的价层电子排布式为_______。
(2)请用电子式表示A、B两元素形成化合物的过程。 。
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________;D的配位数为_______;
②列式计算该晶体的密度___ ____g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_ ____;该化合物中存在一个复杂离子,该离子的化学式为___ ____,配位数是_ __。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省唐山市高三4月第二次模拟理综化学试卷(解析版) 题型:推断题
X、Y、Z、W、R为前四周期原子序数依次增大的五种元素,X、Y、Z、W为同一周期相邻元素,Z元素原子核外电子的运动状态共有8种;R元素与比它核电荷数大的另外两种元素位于第四周期同一族。
(1)X的一种核素用于鉴定文物年代,该核素的符号为____。
(2)X、Y、Z、W四种元素第一电离能由大到小的顺序为____(用元素符号表示)。
(3)用氢键表示式写出W的气态氢化物水溶液中不同种分子间存在的氢键____。
(4)Y的一种氢化物分子中共有18个电子,该分子中存在的共价键类型有____(填选项字母)。
A.非极性键;B.极性键;C. 键;D.
键;D. 键;E.p—p
键;E.p—p 键;F.
键;F. 键;G.
键;G. 键;H.
键;H.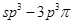 键
键
(5)R的基态原子的价层电子排布式为____,R元素位于周期表的____区。
(6)R单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图所示:

图A中原子堆积方式为 ,A、B中R原子的配位数之比为____。A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com