
| A£® | ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©£»”÷H=-483.6 kJ•mol-1ĒāĘųµÄČ¼ÉÕČČĪŖ”÷H=-241.8 kJ•mol-1 | |
| B£® | ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©£»”÷H£¾0””ŌņŹÆÄ«±Č½šøÕŹÆĪČ¶Ø | |
| C£® | ŅŃÖŖNaOH£Øag£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©£»”÷H=-57.4 kJ•mol-1Ōņŗ¬20.0g NaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7kJµÄČČĮæ | |
| D£® | ¼ŗÖŖ2C£Øs£©+2O2£Øg£©ØT2CO2£Øg£©£»”÷H1 2C£Øs£©+O2£Øg£©ØT2CO£Øg£©£»”÷H2£¬Ōņ”÷H1£¾”÷H2 |
·ÖĪö A£®Č¼ÉÕČČŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļ·Å³öµÄČČĮ棻
B£®ĪļÖŹ¾ßÓŠµÄÄÜĮæŌ½µĶ£¬ĪļÖŹŌ½ĪČ¶Ø£»
C£®ŌŚĻ”ČÜŅŗÖŠ£¬ĒæĖįŗĶĒæ¼ī·“Ӧɜ³É1molĖ®·Å³öµÄČČĮæĪŖÖŠŗĶČČ£¬ÖŠŗĶČȵĵ„Ī»ŹĒkJ/mol£¬µ«ČČĮæµÄµ„Ī»ŹĒkJ£»
D£®ÓĆøĒĖ¹¶ØĀɵƵ½Ņ»Ńõ»ÆĢ¼Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼£¬øł¾ŻÕāøö¹ż³ĢŹĒ·ÅČČĄ“Č·¶ØģŹ±äµÄ“󊔣®
½ā“š ½ā£ŗA£®Ń”ĻīÖŠÉś³ÉµÄĖ®ŹĒĘųĢ壬ӦøĆŹĒŅŗĢ¬Ė®£¬ĖłŅŌ²»ÄÜµĆ³öĒāĘųµÄČ¼ÉÕČČŹĒ241.8 kJ/mol£¬¹ŹA“ķĪó£»
B£®ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0£¬·“Ó¦ŹĒĪüČČ·“Ó¦£¬ŹÆÄ«ÄÜĮæµĶÓŚ½šøÕŹÆ£¬ÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ĖłŅŌŹÆÄ«±Č½šøÕŹÆĪČ¶Ø£¬¹ŹBÕżČ·£»
C£®ŅŃÖŖNaOH£Øag£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H=-57.4 kJ/mol£¬Ōņŗ¬20.0g NaOHĪļÖŹµÄĮæĪŖ0.5molµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7kJµÄČČĮ棬¹ŹC“ķĪó£»
D£®ŅŃÖŖC£Øs£©+O2£Øg£©=CO2£Øg£©”÷H1 ¢Ł£¬C£Øs£©+$\frac{1}{2}$O2£Øg£©=CO£Øg£©”÷H2 ¢Ś£¬¢Ł-¢ŚµĆµ½£ŗCO£Øg£©+$\frac{1}{2}$O2£Øg£©=CO2£Øg£©”÷H1-”÷H2£¬Ņ»Ńõ»ÆĢ¼Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ŹĒ·ÅČČ·“Ó¦£¬ģŹ±äŹĒøŗÖµ£¬ĖłŅŌ”÷H1£¼”÷H2£¬¹ŹD“ķĪó£»
¹ŹŃ”BC£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·½³ĢŹ½£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ČČ»Æѧ·½³ĢŹ½µÄŹéŠ“ŌŌņĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕ»Æѧ·“Ó¦ÓėÄÜĮ¦±ä»ÆµÄ¹ŲĻµ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®


 Ķ¬²½ĒįĖÉĮ·Ļ°ĻµĮŠ“š°ø
Ķ¬²½ĒįĖÉĮ·Ļ°ĻµĮŠ“š°ø æĪæĪĶØæĪ³Ģ±ź×¼Ė¼Ī¬·½·ØÓėÄÜĮ¦ŃµĮ·ĻµĮŠ“š°ø
æĪæĪĶØæĪ³Ģ±ź×¼Ė¼Ī¬·½·ØÓėÄÜĮ¦ŃµĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ż | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ū¢Ż | D£® | ¢Ł¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
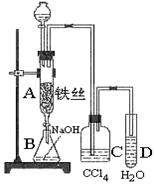 ij»ÆѧæĪĶāŠ”×éÓĆĶ¼×°ÖĆŹ¹±½ÓėŅŗäå·“Ó¦£®ĻČĻņ·ÖŅŗĀ©¶·ÖŠ¼ÓČė±½ŗĶŅŗä壬ŌŁ½«»ģŗĻŅŗĀżĀżµĪČė·“Ó¦Ę÷A£ØAĻĀ¶Ė»īČū¹Ų±Õ£©ÖŠ£®
ij»ÆѧæĪĶāŠ”×éÓĆĶ¼×°ÖĆŹ¹±½ÓėŅŗäå·“Ó¦£®ĻČĻņ·ÖŅŗĀ©¶·ÖŠ¼ÓČė±½ŗĶŅŗä壬ŌŁ½«»ģŗĻŅŗĀżĀżµĪČė·“Ó¦Ę÷A£ØAĻĀ¶Ė»īČū¹Ų±Õ£©ÖŠ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
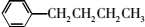 µÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬ŗ¬ÓŠ±½»·ĒŅ±½»·ÉĻŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖֵĽį¹¹¹²ÓŠ£Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£Ø””””£©
µÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬ŗ¬ÓŠ±½»·ĒŅ±½»·ÉĻŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖֵĽį¹¹¹²ÓŠ£Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£Ø””””£©| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8 | B£® | 7 | C£® | 5 | D£® | 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
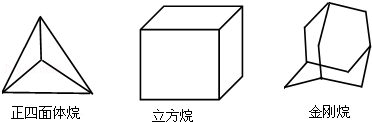
| A£® | 2ÖÖ 4ÖÖ 8ÖÖ | B£® | 2ÖÖ 4ÖÖ 6ÖÖ | C£® | 1ÖÖ 3ÖÖ 6ÖÖ | D£® | 1ÖÖ 3ÖÖ 8ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
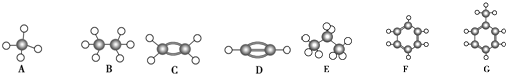
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO32- | B£® | CH4 | C£® | BF3 | D£® | SO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com