
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
(2)由表中数据可知,随温度升高平衡常数增大,说明升高温度平衡正向移动,升高温度平衡向吸热反应方向移动;
(3)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
(4)平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),则平衡常数K=1;
(5)计算该温度下平衡常数,再通入4mol水蒸气,等效为开始通入1molCO、5mol水蒸汽到达的平衡,令平衡时CO2的物质的量为xmol,表示出平衡时各组分物质的量,再根据平衡常数列方程计算.
解答 解:(1)平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,则反应方程式为:CO2(g)+H2(g)?CO(g)+H2O(g),
故答案为:CO2(g)+H2(g)?CO(g)+H2O(g);
(2)由表中数据可知,随温度升高平衡常数增大,说明升高温度平衡正向移动,升高温度平衡向吸热反应方向移动,则正反应为吸热反应,
故答案为:吸热;
(3)A.溶液前后气体物质的量不变,恒温恒容下,容器中压强始终不变,故A错误;
B.混合气体中 c(CO)不变,说明反应到达平衡,故B正确;
C.υ正(H2)=υ逆(H2O)说明水的生成速率与消耗速率相等,反应到达平衡,故C正确;
D.平衡时CO2、CO浓度与二氧化碳转化率有关,平衡时不一定相等,故D错误,
故选:BC;
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),则平衡常数K=1,此时的温度为830℃,
故答案为:830;
(5)某温度下,将CO和水蒸气各1mol置于体积为1L的密闭容器中反应,达到平衡后测得CO2为0.5mol,则生成氢气为0.5mol,该温度下平衡常数K=$\frac{0.5×0.5}{0.5×0.5}$=1,再通入4mol水蒸气,等效为开始通入1molCO、5mol水蒸汽到达的平衡,令平衡时CO2的物质的量为xmol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):1 5 0 0
变化量(mol):x x x x
平衡量(mol):1-x 5-x x x
所以$\frac{x×x}{(1-x)×(5-x)}$=1,解得x=$\frac{5}{6}$
故答案为:$\frac{5}{6}$.
点评 本题考查学生化学平衡常数及其应用、平衡状态判断等,关键是对平衡常数的理解掌握,注意判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol/L Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在:c (Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol/L:c(Na+)=c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) | |
| D. | 常温下,将0.1 mol/L CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液的Kac(H+)值减小到原来的$\frac{1}{10}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④⑤ | C. | ①②③④⑥ | D. | ①②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
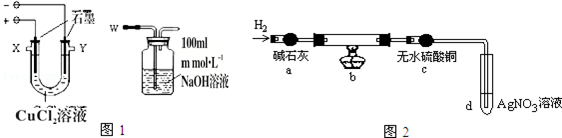
| 物质名称及化学式 | 氯化亚铜CuCl | 碱式氯化铜Cu2(OH)3Cl |
| 性质 | 白色固体、不溶水 | 绿色固体、不溶水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-)时,一定是醋酸过量 | |
| B. | 当溶液中c(CH3COO-)=c(Na+)时,一定是氢氧化钠过量 | |
| C. | 当溶液中c(CH3COO-)=c(Na+)时,醋酸与氢氧化钠恰好完全反应 | |
| D. | 当溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶:500mL、250mL各一个;CuSO4:共120g | |
| B. | 容量瓶:750mL;CuSO4:120g | |
| C. | 容量瓶:1000mL;CuSO4•5H2O:160g | |
| D. | 容量瓶:1000mL;CuSO4:160g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成纤维和光导纤维都属于新型无机非金属材料 | |
| B. | “地沟油”禁止食用,但经过加T处理后,可以用来制取肥皂和生物柴油 | |
| C. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| D. | 2015年10月我国科学家屠呦呦获诺贝尔医学、生理学奖,她发现、创制的药物青篙素( )是治疗疟疾的特效药,青篙素的分子式为C15H22O5 )是治疗疟疾的特效药,青篙素的分子式为C15H22O5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com