
【题目】下列各组物质中,相互间一定互为同系物的是
A. 邻二甲苯和对二甲苯 B. C4H8 O2和C3H6O2
C. C4H10和C20H42 D. C6H5-OH和C6H5-CH2-OH
科目:高中化学 来源: 题型:
【题目】煤燃烧产生的SO2是引起酸雨的原因之一。
(1)每隔一定时间测定某处雨水样品的pH值:
![]()
雨水样品pH值变小的主要原因是____________________。
(2)反应2SO2(g)+O2(g)![]() 2SO3(g)+Q (Q>0),其化学平衡常数表达式_______;升高温度,K____________(填“变大”或者“变小”)。
2SO3(g)+Q (Q>0),其化学平衡常数表达式_______;升高温度,K____________(填“变大”或者“变小”)。
(3)判断已达到化学平衡状态的描述是______(选填编号)。
a.体系的压强不再发生变化 | b.2υ正(SO2)=υ逆(O2) |
c.c(SO2) = c(SO3) | d.气体总质量不再变化 |
(4)防治酸雨常用的措施:向煤中加石灰,减少 SO2的产生。这种煤燃烧后,大部分硫元素最终转化为固体盐是_____________。
(5)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看到浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因:_____________________。
(6)Na2SO3溶液呈碱性,可吸收尾气SO2。Na2SO3溶液呈碱性的原因(用离子方程式表示)_____________________;常温下,0.1mol/L该溶液中离子浓度由大到小排列___________(用离子符号表示)。
(7)常温下,NaHSO3溶液呈酸性,在Na2SO3溶液中滴加稀盐酸至中性时,溶质的主要成分有__________________。(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4]2Fe(SO4)2]是分析化学中的重要试剂。
[查阅资料]隔绝空气加热至500℃时硫酸亚铁铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用下图所示部分装置进行实验(夹持装置略)
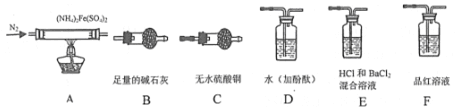
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为________(填装置的字母序号)。
②证明有水蒸气生成的实验现象为___________。
③证明有氨气生成的实验现象为_______________。
④A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4:_________。
(2)探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是_________。
②B的作用是_________。
③实验证明(NH4]2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接甲醇燃料电池以其供电量大、持续时间长而极具发展前景,其工作原理如右图。下列关于它的说法正确的是
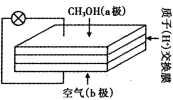
A. 电子自b极经外电路流向a极
B. b极的电极反应式为O2 +4e - +4H+= 2H2O
C. 质子交换膜中的H+流向a极
D. 用该电池电解CuSO4溶液,理论上每生成0.1 molCu消耗氧气1.12 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的的是
A. 用溴水检验汽油中是否含有不饱和脂肪烃
B. 除去苯中混有的苯酚,加入浓溴水,过滤
C. 除去乙醇中混有的水,加入金属钠,蒸馏
D. 乙烷气体中混有乙烯, 通入酸性高锰酸钾溶液,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学镀银法是非金属表面镀银的常用方法。下图是研究化学镀银中银元素利用率的实验装置(夹持仪器略):
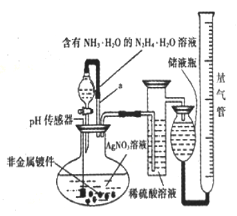
化学镀银中的反应如下:
I:4AgNO3+N2H4·H2O=4Ag↓+N2↑+4HNO3+H2O
Ⅱ:NH3·H2O + HNO3=NH4NO3+H2O
Ⅲ:Ag++2 NH3·H2O= [Ag(NH3)2]++2H2O
(1)写出N2H4的电子式______________。已知稀硝酸的氧化性强于Ag+,N2H4·H2O中加适量氨水的一个重要目的是控制溶液的pH在8~9之间。筒述溶液不能呈酸性的理由___________。
(2)带有导管a的分液漏斗叫恒压漏斗,下列关于恒压漏斗在该实验中的作用说法正确的是____(填选项字母)。
A.防止稀硫酸倒吸进入圆底烧瓶
B.使漏斗中液体顺利流下
C.减小加入液体体积对测量气体体积的误差
D.方便检验装置的气密性
(3)银膜是否均匀致密的关键在于“沉银”速率控制,一般速率越慢,银膜越均匀越致密。简述加入氨水的另外一个目的________。
(4)未被还原的Ag+占总银元素质量比(ψ1)叫非还原损耗,被还原但是没有在镀件上附着沉淀的银占总银元素质量比(ψ2)叫还原损耗。实验中用200 mL 0.100 mol/L AgNO3溶液,加过量的N2H4·H2O,测得相关数据如下:
I:非金属镀件镀前质量为20. 000克,镀后质量(已清洗干燥)为21. 728克;
Ⅱ:量气管收集到的气体折算标准状况体积为106. 400 mL。
则ψ1= __________;ψ2=____________。
(5)化学镀银中常用次磷酸钠(NaH2PO2)做还原剂,已知该反应的氧化产物为磷酸,写出该反应的离子反应方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】游离态的氮经一系列转化可以得到硝酸,如下图所示。
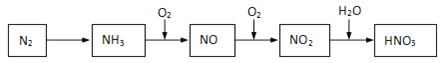
(1)NH3和O2在催化剂作用下反应,其化学方程式是______________。
(2)NO2→HNO3反应中氧化剂和还原剂的物质的量之比为________________。
(3)2NO(g)+O2(g) ![]() 2NO2(g)是制造硝酸的重要反应之一。在800℃时,向容积为1L的密闭容器中充入0.010molNO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一。在800℃时,向容积为1L的密闭容器中充入0.010molNO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。

①2min内,v(O2)=________mol/(L·min)
②800℃时,该反应的化学平衡常数为__________。
③判断该反应达到平衡的依据是(写出2条即可)____________。
④已知:ⅰ.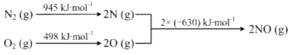
ⅱ.N2(g)+2O2(g)=2NO2(g) ΔH=+68kJ·mol-1,写出NO生成NO2热化学方程式_____________,温度对于NO生成NO2平衡转化率的影响是:___________________。
(4)电解法处理含氮氧化物废气,可以回收硝酸。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极)。请写出电极过程中NO转化为硝酸的电极反应式:______________。
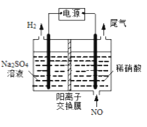
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。TPE的结构简式如图,下列关于TPE的说法正确的是
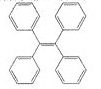
A. TPE属于苯的同系物
B. TPE能发生加成反应,但不能取代反应
C. TPE与化合物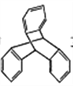 互为同分异构体
互为同分异构体
D. TPE的一氯代物有3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com