


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、只有Cu2+Fe2+ |
| B、只有Fe2+Fe3+ |
| C、一定有Cu2+Fe2+可能有Fe3+ |
| D、一定有Cu2+Fe2+不可能有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、涉及的离子方程式为:Cu+2Fe3+═2Fe2++Cu2+ |
| B、溶液中c(Fe3+):c(Cu2+)=4:3 |
| C、Cu片溶解了1.95g |
| D、此反应可应用于印刷电路板 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(Ca) |
| n(P) |
| n(Ca) |
| n(P) |

| n(Ca) |
| n(P) |
| PH值 | 6.8 | 7.2 | 8.0 | 9.0 | 10.0 | ||
| 产率(%) | 92.6 | 95.3 | 96.7 | 94.6 | 95.6 | ||
|
1.51 | 1.50 | 1.51 | 1.52 | 1.52 |
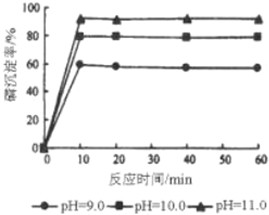
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)氮元素是重要的非金属元素,可形成卤化物、氮化物、叠氮化物及配合物等多种化合物.
(1)氮元素是重要的非金属元素,可形成卤化物、氮化物、叠氮化物及配合物等多种化合物.| 晶格能/kJ?mol-1 | 熔点/℃ | |
| CaO | 3401 | 2927 |
| KCl | 699 | 772 |
| KBr | 689 | 734 |
| KI | 632 | 680 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com