
| A. | 离子半径:Rn+>Zm- | |
| B. | 若Y的最高价氧化物对应的水化物HnY0m为强酸,则X的氢化物沸点一定比Y的氢化物的沸点低 | |
| C. | 若X的气态氢化物能使湿润的石蕊试纸变蓝,则标准状况下,18g Y的氢化物的体积为2.24 L | |
| D. | 若R(OH)n为弱电解质,则W(OH)n+1可与KOH溶液反应 |
分析 A.同周期元素对应的离子,阳离子比阴离子少一个电子层;
B.如Y为N元素,X为C,对应的烃有多种化合物;
C.若X的气态氢化物能使湿润的石蕊试纸变蓝,X为N元素,如Y为O,对应的氢化物为液体;
D.若R(OH)n为弱电解质,则W可为Al.
解答 解:A.同周期元素对应的离子,阳离子比阴离子少一个电子层,阳离子半径小于阴离子,故A错误;
B.如Y为N元素,X为C,对应的烃有多种化合物,可为固态、液态等,沸点较高,故B错误;
C.若X的气态氢化物能使湿润的石蕊试纸变蓝,X为N元素,如Y为O,对应的氢化物为液体,故C错误;
D.若R(OH)n为弱电解质,则W可为Al.氢氧化铝可与KOH等溶液反应,故D正确.
故选D.
点评 本题考查同周期元素的性质的递变规律,为高频考点,侧重考查学生的分析能力,注意把握同周期元素的性质的递变规律和在元素周期表中的可能位置,题目难度不大.


科目:高中化学 来源: 题型:选择题
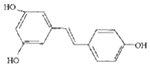 ,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )| A. | 1mol,1mol | B. | 3.5mol,7mol | C. | 3.5mol,6mol | D. | 6mol,7mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
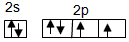 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的醋酸加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
| A. | 完成该实验需用到的实验仪器有试管和胶头滴管 | |
| B. | CCl4在实验中所起的作用是萃取剂 | |
| C. | ③中反应的离子方程式为Cl2+2I-═2Cl-+I2 | |
| D. | 上述三步实验能很好的探究卤素单质的氧化性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
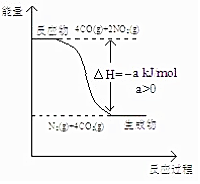 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.
研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
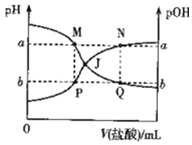
| A. | 曲线PJN表示溶液中pH的变化 | |
| B. | M点水的电离程度比Q点大 | |
| C. | M、P两点的数值之和a+b=14 | |
| D. | pH与pOH交叉点J对应的V(盐酸)=20.00 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 | |
| B. | 煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 | |
| C. | 甲苯和Cl2光照下的反应与乙醇和乙酸反应属于同一类型的反应 | |
| D. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将KI溶液滴入FeCl3溶液中,加入CCl4,振荡、静置 | 下层溶液显紫色 | 还原性:Fe2+<I- |
| B | 将SO2通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
| C | 将稀盐酸滴入Na2SiO3溶液中 | 溶液中出现凝胶 | 非金属性:Cl>Si |
| D | 将稀硫酸滴入淀粉溶液中,加热一段时间,再加入新制的Cu(OH)2悬浊液并加热 | 溶液中未出现砖红色沉淀 | 淀粉未水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com