
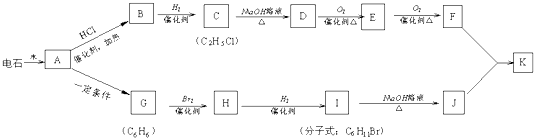
 ��
��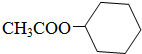 ��
������ ��ʯ�����ɷ�Ӧ����AΪHC��CH����Ȳ��һ������������G�����G�ķ���ʽ��֪��Ӧ��3������Ȳ�����ӳɷ�Ӧ����G����GΪ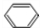 �������巢��ȡ����Ӧ����HΪ
�������巢��ȡ����Ӧ����HΪ ���屽�����������ӳɷ�Ӧ����I�����I�ķ���ʽ��֪��IΪ
���屽�����������ӳɷ�Ӧ����I�����I�ķ���ʽ��֪��IΪ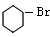 ��I����±������ˮ�ⷴӦ����JΪ
��I����±������ˮ�ⷴӦ����JΪ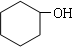 ����Ȳ��HCl�����ӳɷ�Ӧ����B��B��������Ӧ�ӳɷ�Ӧ����C����C�ķ���ʽ��֪��BΪCH2=CHCl��CΪCH3CH2Cl��C����±������ˮ�ⷴӦ����DΪCH3CH2OH��D����������Ӧ����CΪCH3CHO��C��һ������������Ӧ����FΪCH3COOH��F��J����������Ӧ����KΪ
����Ȳ��HCl�����ӳɷ�Ӧ����B��B��������Ӧ�ӳɷ�Ӧ����C����C�ķ���ʽ��֪��BΪCH2=CHCl��CΪCH3CH2Cl��C����±������ˮ�ⷴӦ����DΪCH3CH2OH��D����������Ӧ����CΪCH3CHO��C��һ������������Ӧ����FΪCH3COOH��F��J����������Ӧ����KΪ ���ݴ˽��
���ݴ˽��
��� �⣺��ʯ�����ɷ�Ӧ����AΪHC��CH����Ȳ��һ������������G�����G�ķ���ʽ��֪��Ӧ��3������Ȳ�����ӳɷ�Ӧ����G����GΪ �������巢��ȡ����Ӧ����HΪ
�������巢��ȡ����Ӧ����HΪ ���屽�����������ӳɷ�Ӧ����I�����I�ķ���ʽ��֪��IΪ
���屽�����������ӳɷ�Ӧ����I�����I�ķ���ʽ��֪��IΪ ��I����±������ˮ�ⷴӦ����JΪ
��I����±������ˮ�ⷴӦ����JΪ ����Ȳ��HCl�����ӳɷ�Ӧ����B��B��������Ӧ�ӳɷ�Ӧ����C����C�ķ���ʽ��֪��BΪCH2=CHCl��CΪCH3CH2Cl��C����±������ˮ�ⷴӦ����DΪCH3CH2OH��D����������Ӧ����CΪCH3CHO��C��һ������������Ӧ����FΪCH3COOH��F��J����������Ӧ����KΪ
����Ȳ��HCl�����ӳɷ�Ӧ����B��B��������Ӧ�ӳɷ�Ӧ����C����C�ķ���ʽ��֪��BΪCH2=CHCl��CΪCH3CH2Cl��C����±������ˮ�ⷴӦ����DΪCH3CH2OH��D����������Ӧ����CΪCH3CHO��C��һ������������Ӧ����FΪCH3COOH��F��J����������Ӧ����KΪ ��
��
��1��A����Ȳ��ʵ������ȡA�Ļ�ѧ����ʽ��CaC2+H2O��Ca��OH��2+C2H2����
�ʴ�Ϊ��CaC2+H2O��Ca��OH��2+C2H2����
��2��D��E�Ļ�ѧ����ʽ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
�ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��3��BΪCH2=CHCl�������Ӿ۷�Ӧ���ɾ���ϩ����Ӧ�ķ���ʽΪ��n CH2=CHCl $\stackrel{����}{��}$ ��
��
�ʴ�Ϊ��n CH2=CHCl $\stackrel{����}{��}$ ��
��
��4��������������֪��K�Ľṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5��A��C2H2��ÿĦ����Ȳ��ȫȼ������O2�����ʵ���Ϊ$\frac{2��2+1}{2}$mol=2.5mol��A-K��CH3CHO���Կ���C2H2•H2O������ÿĦ����CH3CHOȫȼ������O2�����ʵ���Ϊ2.5mol��������ʵ�����A��ȫȼ������O2��ͬ��
�ʴ�Ϊ��E��
���� ���⿼���л����ƶϣ��ѶȲ���ע����ݷ�Ӧ��������˳�Ʒ������ƶϣ�ע��Ի���֪ʶ���������գ�


 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.22 mol•��L•min��-1 | B�� | 0.1 mol•��L•min��-1 | ||
| C�� | 0.04 mol•��L•min��-1 | D�� | 0.08 mol•��L•min��-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯī������ʯ�ȶ� | |
| B�� | ���ʯ��ʯī��Ϊͬλ�� | |
| C�� | ʯī�������ڽ��ʯ | |
| D�� | �������Ľ��ʯ��ʯī��ȫȼ�գ�ʯī�ų��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ԣ�A��=0.20mol/��L•min�� | B�� | �ԣ�B��=0.45 mol/��L•min�� | ||
| C�� | �ԣ�C��=0.30 mol/��L•min�� | D�� | �ԣ�D��=0.35 mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�������屽ʱ��������Һ���Ϻ�ӵ�����˿�ķ�Ӧ������ | |
| B�� | ʵ������������ʱ���������뱽��Ϻ��ٵμ�Ũ���� | |
| C�� | ʵ��ʱ��ָ�ϲ�С��մ�ϱ��ӣ�������70�����ϵ���ˮ��ϴ | |
| D�� | ���к��������ʣ���ȥ���ʵķ�����������ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��С��Na��S��O | B�� | �ȶ��ԣ�HI��HBr��HCl��HF | ||
| C�� | ����ǿ����KOH��Ca��0H��2��Mg��OH��2 | D�� | ��ԭ��ǿ����Iһ��CIһ��F? |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������֧�Թܵ���ɫ������ͬ | |
| B�� | A�Թ���Fe��OH��3������� | |
| C�� | ֱ�Ӽ�������Fe2��SO4��3��Һ�ɵõ�Fe2��SO4��3���� | |
| D�� | B�Թ���Fe2��SO4��3���ܷ���ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 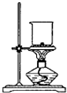 �ص�ȼ��ʵ�� | B�� | 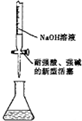 ��ǿ��ζ�ǿ�� | ||
| C�� | 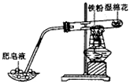 ����H2O��g����Ӧ | D�� | 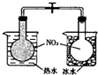 ̽���¶ȶ�ƽ���ƶ���Ӱ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com