
分析 (1)0.01mol/L的NaOH溶液的pH为11,则c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,根据Kw=c(H+)×c(OH-)计算;
(2)混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等;
(3)pH=11的NaOH和pH=2的CH3COOH反应醋酸过量,溶液呈酸性.
解答 解:(1)0.01mol/L的NaOH溶液的pH为11,则c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,Kw=c(H+)×c(OH-)=1×10-13,故答案为:1×10-13;
(2)①混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等,pH=a的NaOH溶液中氢氧根离子浓度=10 a-13 mol/L,pH=b的H2SO4溶液氢离子浓度=10-b mol/L,10 a-13 mol/L×VaL=10-b mol/L×VbL,且a=12,b=2,则Va:Vb=1:10,故答案为:1:10;
②10 a-13 mol/L×VaL=10-b mol/L×VbL,且a+b=11,则Va:Vb=100:1,故答案为:100:1;
(3)pH=11的NaOH和pH=2的CH3COOH反应醋酸过量,溶液呈酸性,故答案为:酸.
点评 本题考查酸碱混合的计算,明确该温度下的Kw及pH与浓度的换算是解答本题的关键,注意酸碱反应的实质即可解答,题目难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大 | |
| B. | 向0.1mol•L-1Na2CO3溶液中加入少量NaOH固体,c(CO32-)与c(Na+)的增大 | |
| C. | NaOH和CH3COONa的混合溶液中,c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 常温下,$\frac{{K}_{W}}{c{(H}^{+})}$=0.1mol•L-1 的溶液中,Na+、K+、CO32-、NO3-、离子可大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物的碱性:Y>W | |
| B. | 气态氢化物的稳定性:X<Z | |
| C. | 原子半径:Y<Z | |
| D. | Y最高价氧化物能与W的最高价氧化物的水化物的溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有金属元素 | |
| B. | 金属元素不可能存在于阴离子中 | |
| C. | 含有非极性键的化合物不一定是共价化合物 | |
| D. | 由两种元素构成的共价化合物分子中的化学键都是极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入10mL 0.01mol•L-1的NaOH溶液 | B. | 加入10mL 0.01mol•L-1的盐酸溶液 | ||
| C. | 加水稀释成100mL | D. | 加入10mL 的水进行稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大N2浓度可以增大反应速率 | |
| B. | 增大H2浓度可以使N2转化率达到100% | |
| C. | 升高温度可以加快反应速率 | |
| D. | 高压条件可以加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.61 | 2.04 | 1.57 | 2.55 | 3.16 | 3.98 | 0.98 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.31 | 3.04 | 0.93 | 3.44 | 2.19 | 2.58 | 1.90 |
| 锂 | X | Y | |
| 失去第1个电子 | 519 | 502 | 580 |
| 失去第2个电子 | 7296 | 4570 | 1820 |
| 失去第3个电子 | 11799 | 6920 | 2750 |
| 失去第4个电子 | 9550 | 11600 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
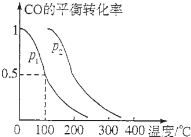
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三氟化氮的电子式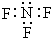 | B. | 水合氢离子电子式: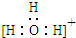 | ||
| C. | 氟离子的结构示意图: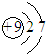 | D. | 中子数为18的硫原子${\;}_{16}^{34}$S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com