
| A、只有② | B、只有③ | C、只有②③ | D、①②③ |
科目:高中化学 来源:2013-2014学年江西省南昌市高二上学期期中测试理科化学试卷(甲)(解析版) 题型:填空题
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。
(l)图中所示反应是______(填“吸热”或“放热”)反应,该反应_______(填“需要”或“不需要”)加热,该反应的△H=_______(用含 、
、 的代数式表示)。
的代数式表示)。
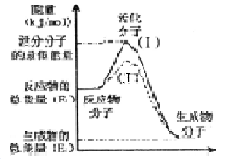
(2)已知热化学方程式:H2(g)
+ O2(g)═H2O(g);△H=-241.5kJ/mol,该反应的活化能为167. 4kJ/mol,则其逆反应的活化能为________________。
O2(g)═H2O(g);△H=-241.5kJ/mol,该反应的活化能为167. 4kJ/mol,则其逆反应的活化能为________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_____________。
查看答案和解析>>
科目:高中化学 来源:2014届湖北省武汉市高二上学期期中考试化学试卷(解析版) 题型:填空题
(7分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。

(1)图中所示反应是_________(填“吸热”或“放热”,1分)反应,该反应________(填“需要”或“不需要”,1分)加热,该反应的△H=____________(用含E1、E2的代数式表示,1分)。
(2)已知热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H=-241.5 kJ/mol,该反应的活化能为167.4 kJ/mol,则其逆反应的活化能为_________________(2分)。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_____________________(2分)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省葫芦岛市五校协作体高三上学期模拟考试化学卷 题型:填空题
(10分,每空2分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。

(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应________(填“需要” 或“不需要”)加热,该反应的△H=____________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+0.5 O2(g)=H2O(g);△H=-241.8 kJ/mol
该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为____________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(12分)(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察下图,然后回答问题:
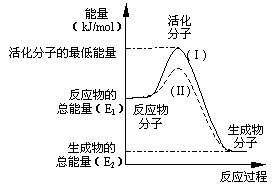 ①图中所示反应是_____________(填“吸热”
①图中所示反应是_____________(填“吸热”
或“放热”)反应,该反应____________
(填“需要”或“不需要”)加热,该反应的
△H=____________(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+1/2O2(g)=H2O(g);
△H=-241.8 kJ/mol。该反应的活化能为
167.2kJ/mol,则其逆反应的活化能为____________。
③对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,
活化能大大降低,活化分子的百分数增多,反应速率明显加快,你认为最可能的原因是_________ ____________________________________________。
(2)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。
①有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ/mol
B、CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
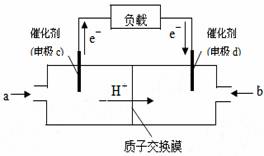 ②下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。
②下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。
甲醇在催化剂作用下提供质子和电子,电子经外电路、
质子经内电路到达另一极与氧气反应,电池总反应为:
2CH3OH+3O2=2CO2+4H2O。则c电极是
(填“正极”或“负极”),c电极上发生的电极反应式
是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com