
| A. | H2 和 D2 互为同位素 | |
| B. | CH3-CH2-NO2和H2N-CH2-COOH互为同分异构体 | |
| C. | 甲苯和 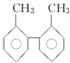 互为同系物 互为同系物 | |
| D. | 金刚石、石墨和“足球烯”(分子式为 C60)为同素异形体 |
分析 A.同位素的研究对象为原子,H2和D2都是氢气分子;
B.具有相同分子式、不同结构的物质之间互为同分异构体;
C.同系物必须具有相似结构,二者含有苯环数目不同,不属于同系物;
D.同种元素形成的不同单质互为同素异形体.
解答 解:A.H、D互为同位素,而H2和D2都是氢气分子,不属于同位素,故A错误;
B.CH3-CH2-NO2和H2N-CH2-COOH的分子式相同、结构不同,二者互为同分异构体,故B正确;
C.甲苯和  含有苯环数目不同,则二者结构不同,一定不属于同系物,故C错误;
含有苯环数目不同,则二者结构不同,一定不属于同系物,故C错误;
D.金刚石、石墨和“足球烯”(分子式为 C60)都是碳元素形成的不同单质,三者互为同素异形体,故D正确;
故选BD.
点评 本题考查了同位素、同分异构体、同系物、同素异形体的判断,题目难度不大,明确同位素、同分异构体、同系物、同素异形体的概念为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


科目:高中化学 来源: 题型:实验题
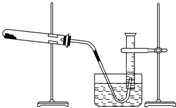 某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应前酸、碱溶液的温度要相同 | |
| B. | 环形玻璃棒搅拌能加快反应速率,减小实验误差 | |
| C. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| D. | 为了使反应更完全,可以使酸或碱适当过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
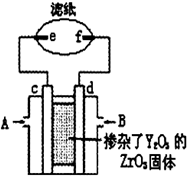 向新型燃料电池的两极分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传到O2-,图中滤纸用含有酚酞的氯化钠溶液浸泡过,c、d、e、f均为惰性电极,工作后e极周围变红,下列叙述正确的是( )
向新型燃料电池的两极分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传到O2-,图中滤纸用含有酚酞的氯化钠溶液浸泡过,c、d、e、f均为惰性电极,工作后e极周围变红,下列叙述正确的是( )| A. | c极为正极,A处通入甲烷气体 | B. | d极的反应式为O2+2H2O+4e-=4OH- | ||
| C. | 固体电解质中O2-由d极向c极移动 | D. | e极上发生氧化反应,pH上升 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
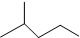 表示的分子式C6H14;名称2-甲基戊烷.
表示的分子式C6H14;名称2-甲基戊烷.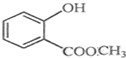 中含有的官能团的名称为酚羟基、酯基.
中含有的官能团的名称为酚羟基、酯基. .3-甲基-2-乙基-1-戊烯结构简式为CH3CH(CH3)CH2C(CH2CH3)=CH2.
.3-甲基-2-乙基-1-戊烯结构简式为CH3CH(CH3)CH2C(CH2CH3)=CH2.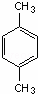 名称为对二甲苯.
名称为对二甲苯.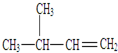 名称为3-甲基-1-丁烯.
名称为3-甲基-1-丁烯.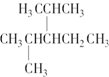 名称为2,4-二甲基-3--乙基戊烷.
名称为2,4-二甲基-3--乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
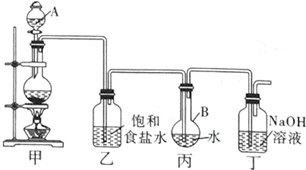
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
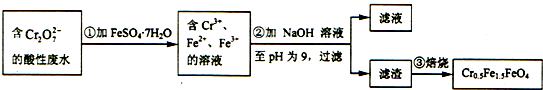
| A. | 根据第①步反应可知还原性:Cr3+大于Fe2+ | |
| B. | 第②步过滤得到的滤渣中主要成分为Cr(OH)3、Fe(OH)2,不含Fe(OH)3 | |
| C. | 欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入27.8g FeSO4•7H2O | |
| D. | 第③步高温焙烧过程用到的主要实验仪器中属于硅酸盐质的有:酒精灯、蒸发皿、泥三角 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com