
| A. | 石油分馏是物理变化,可得到汽油、煤油和柴油等产品 | |
| B. | 石油的催化重整和煤的干馏均可以得到芳香烃 | |
| C. | 石油裂解的目的主要是为了得到更多的汽油 | |
| D. | 煤、石油、天然气既是一次能源,又是不可再生能源 |
分析 A、石油的分馏是根据物质的沸点不用进行分离的;
B、煤焦油中含有芳香烃,石油催化重整可获得芳香烃;
C、石油裂解的目的是获得乙烯;
D、煤、石油和天然气为化石燃料,短期内不能再生.
解答 解:A、石油的分馏是根据物质的沸点不用进行分离的,可得汽油、煤油和柴油,属于物理变化,故A正确;
B、煤焦油中含有芳香烃,而煤焦油是通过煤的干馏得到的,石油催化重整可获得芳香烃,故B正确;
C、石油裂解的目的是获得乙烯,裂化的目的是获得轻质油,故C错误;
D、煤、石油和天然气为化石燃料,短期内不能再生,且没有经过人为的再加工,故为一次能源,且不能再生能源,故D正确.
故选C.
点评 本题考查石油分馏和加工、煤的干馏等,题目难度不大,注意煤焦油中含有芳香烃,石油催化重整可获得芳香烃.


科目:高中化学 来源: 题型:选择题
| A. | 向Ag(NH3)2NO3溶液中加人盐酸:Ag(NH3)++2H+═Ag++2NH4+ | |
| B. | 向 Na202 中加人足量水:2Na202+2H20═4Na++40H-+02↑ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++30H-═Al(0H)3↓ | |
| D. | 向 Ca(HC03)2溶液中加入澄淸石灰水:Ca2++2HC03-+20H-═CaC03↓+C032-+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 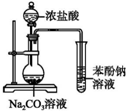 证明酸性:盐酸>碳酸>苯酚 | B. |  溴水褪色一定产生了乙烯 | ||
| C. |  分离溴乙烷和水 | D. | 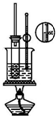 实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | E、C、D、B、A | B. | B、A、E、D、C | C. | E、B、A、D、C | D. | A、B、C、D、E |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com