

| Ąė×Ó | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| ÅضČ/mol•L-1 | 4”Į10-6 | 6”Į10-6 | 2”Į10-5 | 4”Į10-5 | 3”Į10-5 | 2”Į10-5 |
·ÖĪö £Ø1£©ČČ»Æѧ·½³ĢŹ½½įŗĻøĒĖ¹¶ØĀɼĘĖć·ÖĪöµĆµ½ČČ»Æѧ·½³ĢŹ½£»ŅĄ¾Ż·“Ó¦Ē°ŗóŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ·ÖĪö¼ĘĖćŃõ»Æ»¹Ō·“Ó¦µÄµē×Ó×ŖŅĘ£»
£Ø2£©ėĀ·Ö×ÓÖŠĆæøöNŌ×ÓŠĪ³É3øö¹²¼Ū¼ü£¬ĒŅ»¹ŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪČ·¶ØNŌ×ÓŌÓ»ÆĄąŠĶ£»¹żŃõ»ÆĒāĪŖ¹²¼Ū»ÆŗĻĪļ£¬¾Ż“ĖŹéŠ“µē×ÓŹ½£»
£Ø3£©ĻČøł¾ŻČÜŅŗÖŠµēŗÉŹŲŗć¼ĘĖćĒāĄė×ÓµÄÅØ¶Č£¬Č»ŗóĒó³öpH£»
£Ø4£©¢ŁĢ¼ŗĶĖ®ÕōĘų·“Ӧɜ³ÉŅ»Ńõ»ÆĢ¼ŗĶĒāĘų£¬Ė®ĆŗĘųÖŠŅ»Ńõ»ÆĢ¼”¢ĒāĘų¾ßÓŠ»¹ŌŠŌ£¬æÉŅŌ»¹Ō½šŹōŃõ»ÆĪļ£»
¢Ś¶žŃõ»ÆĮņŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļæÉŅŌŗĶ¼ī·“Ó¦£¬¶žŃõ»ÆĮņČÜÓŚĖ®µĆŃĒĮņĖį£¬ĖįŠŌĒæÓŚĢ¼Ėį£¬ĖłŅŌæÉŅŌŗĶĢ¼ĖįÄĘČÜŅŗ·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©¢ŁN2H4£Øl£©+2H2O2£Øl£©ØTN2£Øg£©+4H2O£Øg£©”÷H=-641.6kJ/mol
¢ŚH2O£Øl£©ØTH2O£Øg£©”÷H=+44kJ/mol£»
ŅĄ¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł-¢Ś”Į4µĆµ½£ŗN2H4£Øl£©+2H2O2£Øl£©=N2 £Øg£©+4H2O £Øl£©”÷H=-817.6 kJ/mol£»ŅĄ¾Ż·“Ó¦Ē°ŗóŌŖĖŲ»ÆŗĻ¼Ū±ä»ÆæÉÖŖ£¬N2H4”«N2”«4e-£»3.2gŅŗĢ¬ėĀĪļÖŹµÄĮæ=$\frac{3.2g}{32g/mol}$=0.1mol£»ŅĄ¾Żµē×ÓŹŲŗć¼ĘĖćµĆµ½×ŖŅʵē×ÓĪŖ0.4mol£»
¹Ź“š°øĪŖ£ŗ0.4mol£» N2H4£Øl£©+2H2O2£Øl£©=N2 £Øg£©+4H2O £Øl£©”÷H=-817.6 kJ/mol£»
£Ø2£©ėĀ·Ö×ÓÖŠĆæøöNŌ×ÓŠĪ³É3øö¹²¼Ū¼ü£¬ĒŅ»¹ŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬Ęä¼Ū²ćµē×Ó¶ŌøöŹżŹĒ4£¬ĖłŅŌµŖŌ×ÓµÄŌӻƷ½Ź½ĪŖsp3Ōӻƣ¬¹żŃõ»ÆĒāĪŖ¹²¼Ū»ÆŗĻĪļ£¬¾Ż“ĖŹéŠ“µē×ÓŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗsp3Ōӻƣ» £»
£»
£Ø3£©¹Ū²ģ±ķøńÖŠ·¢ĻÖNH4+Ė®½āĻŌĖįŠŌ£¬PM2.5µÄĖį¼īŠŌĪŖĖįŠŌ£»ŹŌŃłµÄpHÖµøł¾ŻČÜŅŗÖŠµēŗÉŹŲŗć£ŗc£ØH+£©+c£ØK+£©+c£ØNa+£©+c£ØNH4+£©=2c£ØSO42-£©+c£ØNO3-£©+c£ØCl-£©¼ĘĖćH+Ąė×ÓÅضČĪŖ10-4£¬øĆŃł±¾µÄpH=4£¬
¹Ź“š°øĪŖ£ŗ4£»
£Ø4£©¢Ł½¹ĢæÓėĖ®ÕōĘųøßĪĀ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗC+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$CO+H2£¬Ņ»Ńõ»ÆĢ¼æÉŅŌ»¹ŌŃõ»ÆĢśÉś³ÉĢś×ö»¹Ō¼Į£¬
¹Ź“š°øĪŖ£ŗC+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$CO+H2£»×ö»¹Ō¼ĮŅ±Į¶½šŹō£»
¢Śa£®¶žŃõ»ÆĮņŹĒĖįŠŌŃõ»ÆĪļĖłŅŌ¾ßÓŠĖįŠŌŃõ»ÆĪļµÄĶØŠŌÄܹ»Óė¼ī·“Ó¦£ŗŗĶĮņĖįÄĘ²»·“Ó¦£¬¹Źa“ķĪó£»
b£®¶žŃõ»ÆĮņĖ®ČÜŅŗŹĒŃĒĮņĖįĖłŅŌŅ²Äܹ»ÓėĢ¼ĖįÄĘ·“Ó¦£ŗSO2+Na2CO3=Na2SO3+CO2”ü£¬æÉŅŌÓĆĢ¼ĖįÄĘČÜŅŗ×öĻ“µÓ¼Į£¬¹ŹbÕżČ·£»
c£®¶žŃõ»ÆĮņÓėĀČ»ÆøĘČÜŅŗ²»·“Ó¦£¬²»ÄÜÓĆĀČ»ÆøĘČÜŅŗĪüŹÕ¶žŃõ»ÆĮņ£¬¹Źc“ķĪó£»
d£®¶žŃõ»ÆĮņÓėĮņĒā»ÆÄĘČÜŅŗ·“Ӧɜ³ÉĮņµ„ÖŹ£¬ĖłŅŌæÉŅŌÓĆĮņĒā»ÆÄĘČÜŅŗĪüŹÕ£¬¹ŹdÕżČ·£»
¹ŹŃ”£ŗbd£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½µÄŹéŠ“·½·Ø”¢øĒĖ¹¶ØĀɵļĘĖćÓ¦ÓĆ£¬Ńõ»Æ»¹Ō·“Ó¦µÄµē×Ó×ŖŅĘ¼ĘĖć”¢ČÜŅŗpHÖµµÄ¼ĘĖć£¬ÕĘĪÕøĒĖ¹¶ØĀɵÄŗ¬Ņ壬Ć÷Č·ČÜŅŗÖŠµēŗÉŹŲŗć¹ęĀɼ°pH¼ĘĖć¹«Ź½ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4ŗĶC4H8 | B£® | CH4ŗĶC3H6 | C£® | C2H6 ŗĶC3H6 | D£® | C2H6 ŗĶC4H8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
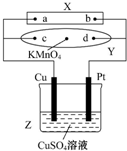 Ķ¼ÖŠXĪŖµēŌ“£¬YĪŖ½žĶø±„ŗĶŹ³ŃĪĖ®ŗĶ·ÓĢŖŹŌŅŗµÄĀĖÖ½£¬ĀĖÖ½ÖŠŃėµĪÓŠŅ»µĪKMnO4ČÜŅŗ£¬ĶصēŗóYÖŠŃėµÄ×ĻŗģÉ«°ßĻņd¶ĖĄ©É¢£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
Ķ¼ÖŠXĪŖµēŌ“£¬YĪŖ½žĶø±„ŗĶŹ³ŃĪĖ®ŗĶ·ÓĢŖŹŌŅŗµÄĀĖÖ½£¬ĀĖÖ½ÖŠŃėµĪÓŠŅ»µĪKMnO4ČÜŅŗ£¬ĶصēŗóYÖŠŃėµÄ×ĻŗģÉ«°ßĻņd¶ĖĄ©É¢£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | ĀĖÖ½ÉĻcµćø½½ü»į±äŗģÉ« | B£® | Cuµē¼«ÖŹĮæ¼õŠ”£¬Ptµē¼«ÖŹĮæŌö“ó | ||
| C£® | ZÖŠČÜŅŗµÄpHĻČ¼õŠ”£¬ŗóŌö“ó | D£® | ČÜŅŗÖŠµÄSO42-ĻņCuµē¼«¶ØĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĆŗµÄøÉĮó°üĄØ»Æѧ±ä»ÆŗĶĪļĄķ±ä»Æ | |
| B£® | ÕÓĘų£ØÖ÷ŅŖ³É·ÖŹĒCH4£©ŹĒæÉŌŁÉśÄÜŌ“ | |
| C£® | ČĖĄąĄūÓƵÄÄÜŌ“¶¼ŹĒĶعż»Æѧ·“Ó¦»ńµĆµÄ | |
| D£® | ŹÆÓĶŹĒÓÉ1-50øöĢ¼Ō×ÓµÄĶéĢžŗĶ»·ĶéĢž×é³ÉµÄ»ģŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH2=CHCH£ØBr£©CH2Br | B£® | CH2=CH£ØBr£©CHCH2Br | C£® | CH2=CH2CH2CHBr2 | D£® | CH Br2CH=CHCH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
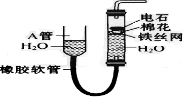 ČēĶ¼ÖŠµÄŹµŃé×°ÖĆæÉÓĆÓŚÖĘČ”ŅŅČ²£® ĒėĢīæÕ£ŗ
ČēĶ¼ÖŠµÄŹµŃé×°ÖĆæÉÓĆÓŚÖĘČ”ŅŅČ²£® ĒėĢīæÕ£ŗ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶ŌČ¼Ćŗ½ųŠŠĶŃĮņ | |
| B£® | ¶Ōŗ¬SO2”¢NO2µČ¹¤Ņµ·ĻĘų½ųŠŠĪŽŗ¦“¦Ąķŗó£¬ŌŁÅŷŵ½“óĘųÖŠ | |
| C£® | ČĖ¹¤ŹÕ¼ÆĄ×µē×÷ÓĆĖł²śÉśµÄµŖµÄŃõ»ÆĪļ | |
| D£® | ·É»ś”¢Ęū³µµČ½»Ķع¤¾ß²ÉÓĆĒå½ąČ¼ĮĻ£¬ČēĢģČ»Ęų”¢¼×“¼µČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 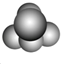 ¼×ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« | |
| B£® |  ŅŅæÉÓėäåĖ®·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ« | |
| C£® |  ±ūÖŠµÄĢ¼Ģ¼¼üŹĒĢ¼Ģ¼µ„¼üŗĶĢ¼Ģ¼Ė«¼ü½»Ģę½įŗĻ | |
| D£® |  ¶”ŌŚCu“ß»Æ×÷ÓĆĻĀæÉÓėŃõĘų·¢ÉśČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com