
【题目】下列有关说法不正确的是
A.根据化合物在水溶液或熔融状态下是否导电,将化合物分为电解质和非电解质
B.氨气的水溶液能够导电,因此NH3是电解质
C.电解质溶液的导电能力与溶液中离子浓度及离子所带电荷多少有关
D.溶液与胶体的本质区别是分散质颗粒直径大小
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是
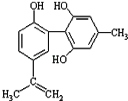
A.该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.该分子中的所有碳原子不可能共平面
D.1mol此物质分别与浓溴水和H2反应时最多消耗Br2和H2为4mol和7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列选项的编号和曲线的编号一一对应,其中描述错误的是
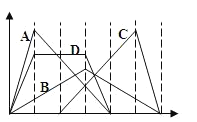
A. 向NaAlO2溶液中逐渐滴入HCl至过量
B. 向澄清石灰水中通入CO2至过量
C. 向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D. 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]22H2O部分信息如下:
物理性质 | 化学性质 |
红棕色晶体,微溶于乙醇,难溶于冷水和乙醚(易挥发的有机溶剂) | 具有强还原性,易被氧化 |
制备原理:2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)=[Cr(CH3COO)2]22H2O(s)。
某兴趣小组设计实验制备[Cr(CH3COO)2]22H2O(s)。

回答下列问题:
(1)仪器A的名称是_____。
(2)检查装置B气密性的操作方法是_____。
(3)加入盐酸后,关闭K1,打开K2,将装置B中的导管抽出液面以上一段时间,目的是____。反应开始后,从装置B中看到的现象是溶液由深绿色(Cr3+)变为亮蓝色(Cr2+),且有气泡产生。写出装置B中发生的非置换反应的离子方程式:_____。
(4)当氢气的放出速率较快时,为了使装置B中溶液进入装置C中,宜采取的操作是_____;装置D中导管口水封的目的是_____。
(5)将装置C中所得产品提纯,其操作依次为过滤、去氧水洗涤、乙醚洗涤。相对乙醇或水,用乙醚洗涤的优点有______。
(6)测定产品纯度:取ag产品溶于蒸馏水,通入足量空气,充分反应后,加入过量氢氧化钠溶液,过滤、洗涤、灼烧、称重。得Cr2O3质量为mg(假设杂质不参与反应),[Cr(CH3COO)2]22H2O(s)的摩尔质量为Mg·mol-1。测得产品纯度为____ %。(用含a、m、M的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )

A. 生成乙烯的速率:v(N)一定大于v(M) B. 该反应的逆反应为吸热反应
C. 平衡常数:KM>KN D. 当温度高于250 ℃,升高温度,催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A.C燃烧的热化学方程式为:C(s)+1/2O2(g)=CO(g) △H = 110.5kJ·mol-1
B.由H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1可知,若将含1molCH3COOH的稀溶液与含1molNaOH的稀溶液混合,放出的热量小于57.3kJ
C.碳酸氢钠水解的离子方程式:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D.500℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关《化学反应原理》的内容说法不正确的是
A. 应用盖斯定律,可计算某些难以直接测量的反应的焓变
B. 向FeCl3与CuCl2溶液中加入碱式碳酸铜调节pH可以除去溶液中的FeCl3
C. 使用催化剂,可以增大活化分子百分数,加快反应速率
D. 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中正确的是
A. 提取溶解在水中的少量碘:加入酒精振荡、静置分层后,取出有机层再分离
B. 下图所示装置都适宜于HCl气体尾气吸收
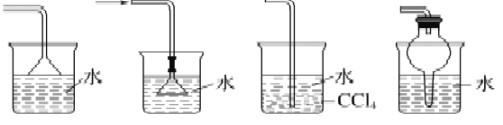
C. 酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差;在用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体。
D. 除去酸性MgCl2溶液中少量的FeCl3:加入足量的Mg(OH)2 并过滤;除去NH4Cl溶液中的FeCl3,可向溶液中加入氨水调节pH .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加。
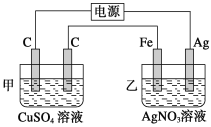
(1)写出甲中发生反应的化学方程式:____________________________。
(2)写出乙中两极发生的电极反应式。
阳极:_______________;阴极:_____________________。
Ⅱ.在一定温度下,将2mol A和2mol B两种气体相混合于容积为2 L的某密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),2min末反应达到平衡状态,生成了0.6mol D,并测得C的浓度为0.3mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.6mol D,并测得C的浓度为0.3mol/L,请填写下列空白:
(1)x值等于__________。
(2)A的转化率为__________。
(3)生成D的反应速率为________________。
(4)达平衡后保持容器内气体压强不变,向其中加入He(He不参加反应),则平衡______移动(填“正向”“逆向 “或”“不”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com