
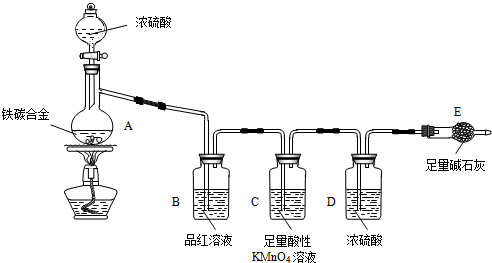
分析 由实验装置图可知,装置A中浓硫酸和铁、碳在加热的条件下反应生成了二氧化碳和二氧化硫,装置B品红溶液是检验二氧化硫气体的,装置C足量的高锰酸钾溶液是除掉二氧化硫的,装置D是用于干燥二氧化碳气体,最后得到干燥的二氧化碳被实验装置E中足量的碱石灰吸收,
(1)依据装置中的压强变化恒容液面变化分析检验,最后导气管插入水,加热发生装置导气管冒气泡,停止加热上升一段水柱;
(2)根据mg铁碳合金,加入过量浓硫酸,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则可求出mg铁碳合金中含碳元素的质量进而求出铁的质量分数;
(3)装置C是利用高锰酸钾的强氧化性吸收二氧化硫气体;
(4)E装置后再连接一个盛碱石灰的干燥管防止空气中的二氧化碳、水蒸气进入干燥管;
(5)装置中生成的二氧化碳不能全部被碱石灰吸收;
(6)常温下铁在浓硫酸中钝化,碳和浓硫酸在加热条件下才能反应;
(7)铁和过量浓硫酸加热反应生成硫酸铁、二氧化硫和水.
解答 解:(1)关闭分液漏斗的活塞,在E装置后面连上一根导管,然后把最后导气管插入水,加热发生装置导气管冒气泡,停止加热上升一段水柱证明装置气密性好,
故答案为:将导气管插入水中,加热烧瓶,导气管冒气泡,停止加热有一段水柱上升;
(2)称取mg铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则mg铁碳合金中含碳元素的质量为$\frac{12b}{44}$g=$\frac{3b}{11}$g,则含铁的质量为mg-$\frac{3b}{11}$g,铁的质量分数为$\frac{m-\frac{3b}{11}}{m}$×100%=$\frac{11m-3b}{11m}$×100%,
故答案为:$\frac{11m-3b}{11m}$×100%;
(3)装置C是利用高锰酸钾溶液的强氧化性吸收二氧化硫,5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,
故答案为:吸收除去二氧化硫;
(4)E中所装试剂为碱石灰,可吸收空气中CO2、H2O使b增大,改进的方法是增加一个盛碱石灰的干燥管防止空气中的二氧化碳和水进入,
故答案为:E装置后再连接一个盛碱石灰的干燥管;
(5)装置中生成的二氧化碳不能全部被碱石灰吸收会导致测定结果偏低,
故答案为:反应产生的CO2气体未能完全排到装置E中,导致b偏低;
(6)往A中滴加足量的浓硫酸,未点燃酒精灯前,A、B均无明显现象,常温下铁在浓硫酸中钝化,碳和浓硫酸在加热条件下才能反应,
故答案为:常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应,故无明显现象;
(7)铁和过量浓硫酸加热反应生成硫酸铁、二氧化硫和水,反应的化学方程式为:2Fe+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O,
故答案为:2Fe+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O.
点评 本题考查了物质性质的探究实验方法,装置的特征分析,流程反应和试剂作用是解题关键,题目难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH═CHCH2CH3 | B. | CH2═CHCH2CH2CH3 | ||
| C. | CH3CH═CHCH2CH2CH3 | D. | 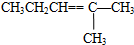 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 异戊二烯CH2═C(CH3)CH═CH2与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷(CH3CH2CHClCH3)与NaOH乙醇溶液共热发生消去反应 | |
| C. | 甲苯在一定条件下生成一硝基取代物的反应 | |
| D. | 邻羟基苯甲酸与NaHCO3溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 将Fe3O4固体溶于HI溶液中:Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| C. | 将氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向FeBr2溶液中通入少量的氯气:2Br-+Cl2=2Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
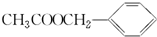 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: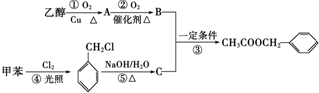
 .
.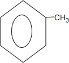 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl.
+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气和臭氧互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$ He和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{4}$ He的最外层电子数为2,所以${\;}_{2}^{3}$He具有较强的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
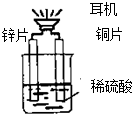
| A. | 铜片表面有气泡产生 | |
| B. | 装置中存在化学能→电能→声能的能量转化 | |
| C. | 如果将铜片换成铁片,电路中的电流方向将改变 | |
| D. | 如果将锌片换成铁片,耳机还能发声 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
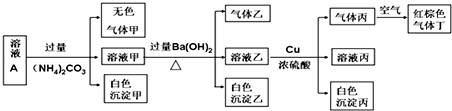
| A. | 沉淀乙一定有BaCO3,可能有BaSO4 | |
| B. | 该溶液A中一定有NO3-、Al3+、SO42-、Cl- | |
| C. | 实验消耗Cu 14.4 g,则生成气体丙为3.36L | |
| D. | 生成的甲、乙、丙气体均为无色的易溶于水气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com