
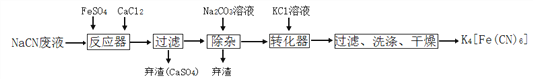
”¾ĢāÄæ”æŃĒĢśĒč»Æ¼ŲK4[Fe(CN)6]£¬Ė×Ćū»ĘŃŖŃĪ£¬æÉČÜÓŚĖ®£¬²»ČÜÓŚŅŅ“¼”£ŌŚ»ÆѧŹµŃ锢µē¶Ę”¢Ź³Ę·Ģķ¼Ó¼Į”¢ÉÕÖĘĒą»Ø“ÉŹ±æÉÓĆÓŚ»ę»µČ·½ĆęÓŠ¹ć·ŗÓĆĶ¾”£ŅŃÖŖHCNŹĒŅ»ÖÖ¼«ČõµÄĖį£¬ĻÖÓŠŅ»ÖÖÓĆŗ¬NaCNµÄ·ĻĖ®ŗĻ³É»ĘŃŖŃĪµÄÖ÷ŅŖ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
£Ø1£©³£ĪĀĻĀ£¬NaCNĖ®ČÜŅŗµÄpH _______ 7(Ģī”°£¾”±”¢”°£½”±”¢”°£¼”±)£¬ŹµŃéŹŅÓĆNaCN¹ĢĢåÅäÖĘNaCNČÜŅŗŹ±£¬Ó¦ĻČ½«ĘäČÜÓŚ_______ČÜŅŗ£¬ŌŁÓĆÕōĮóĖ®Ļ”ŹĶ”£
£Ø2£©·“Ó¦Ę÷ÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ _____________________________”£
£Ø3£©Į÷³ĢÖŠ¼ÓČėNa2CO3ČÜŅŗŗó¹żĀĖ³żČ„ĘśŌü£¬¹żĀĖŠčŅŖµÄ²£Į§ŅĒĘ÷ÓŠÉÕ±”¢Ā©¶·”¢______”£
£Ø4£©×Ŗ»ÆĘ÷ÖŠÉś³ÉK4[Fe(CN)6]µÄ·“Ó¦ĄąŠĶŹĒ________________£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Čܽā¶Č£ŗK4[Fe(CN)6] _______ Na4[Fe(CN)6](Ģī”°£¾”±”¢”°£½”±”¢”°£¼”±) £¬¹żĀĖŗóĻ“µÓK4[Fe(CN)6]Ź¹ÓƵďŌ¼ĮŹĒ________________”£
£Ø5£©ŹµŃéŹŅ³£ÓĆK4[Fe(CN)6]¼ģŃéFe3+£¬Éś³ÉÄŃČÜŃĪKFe[Fe(CN)6]£¬ŹŌŠ“³öÉĻŹö·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ _________________________”£
£Ø6£©ŗ¬ÓŠ14.7kg NaCNµÄ¹¤Ņµ·ĻĖ®æÉÉś²ś³ö9.2kgµÄK4[Fe(CN)6]£¬ŌņK4[Fe(CN)6]µÄ²śĀŹŹĒ_______”£
”¾“š°ø”æ £¾ ÅØNaOH 6NaCN+FeSO4+CaCl2£½Na4[Fe(CN)6]+ CaSO4”ż+2NaCl ²£Į§°ō ø“·Ö½ā·“Ó¦ £¼ ŅŅ“¼ K++Fe3++ [Fe(CN)6]4££½KFe[Fe(CN)6]”ż 50£„
”¾½āĪö”æ£Ø1£©HCNĪŖ¼«ČõµÄĖį£¬NaCNĪŖĒæ¼īČõĖįŃĪ£¬CN-+H2O![]() HCN+OH-£¬Ė®ČÜŅŗĻŌ¼īŠŌ£¬ŌņPH>7£¬ÅäÖĘNaCNČÜŅŗ£¬ĪŖ·ĄÖ¹Ęä·¢ÉśĖ®½ā£¬ĻČČܽāµ½ÅØNaOHČÜŅŗÖŠ£¬Č»ŗó¼ÓĖ®Ļ”ŹĶ£»£Ø2£©øł¾ŻĮ÷³ĢĶ¼£¬6NaCN+FeSO4+CaCl2£½Na4[Fe(CN)6]+ CaSO4”ż+2NaCl£»£Ø3£©¹żĀĖŠčŅŖÓƵ½²£Į§ŅĒĘ÷ÓŠĀ©¶·”¢²£Į§°ō”¢ÉÕ±£»£Ø4£©×Ŗ»ÆĘ÷ÖŠ·¢ÉśµÄ·“Ó¦ŹĒ£ŗNa4[Fe(CN)6]+ KCl= K4[Fe(CN)6]+ NaCl£¬“Ė·“Ó¦ŹōÓŚø“·Ö½ā·“Ó¦£¬µĆ³öK4[Fe(CN)6]Čܽā¶ČŠ”ÓŚNa4[Fe(CN)6]£¬ŃĒĢśĒč¼ŲæÉČÜÓŚĖ®£¬²»ČÜÓŚŅŅ“¼£¬Ņņ“ĖĻ“µÓ³ĮµķÓĆŅŅ“¼£»£Ø5£©øł¾ŻŠÅĻ¢£¬K++Fe3++ [Fe(CN)6]4££½KFe[Fe(CN)6]”ż£»£Ø6£©øł¾ŻCN-ŹŲŗć£¬n[K4[Fe(CN)6]]=
HCN+OH-£¬Ė®ČÜŅŗĻŌ¼īŠŌ£¬ŌņPH>7£¬ÅäÖĘNaCNČÜŅŗ£¬ĪŖ·ĄÖ¹Ęä·¢ÉśĖ®½ā£¬ĻČČܽāµ½ÅØNaOHČÜŅŗÖŠ£¬Č»ŗó¼ÓĖ®Ļ”ŹĶ£»£Ø2£©øł¾ŻĮ÷³ĢĶ¼£¬6NaCN+FeSO4+CaCl2£½Na4[Fe(CN)6]+ CaSO4”ż+2NaCl£»£Ø3£©¹żĀĖŠčŅŖÓƵ½²£Į§ŅĒĘ÷ÓŠĀ©¶·”¢²£Į§°ō”¢ÉÕ±£»£Ø4£©×Ŗ»ÆĘ÷ÖŠ·¢ÉśµÄ·“Ó¦ŹĒ£ŗNa4[Fe(CN)6]+ KCl= K4[Fe(CN)6]+ NaCl£¬“Ė·“Ó¦ŹōÓŚø“·Ö½ā·“Ó¦£¬µĆ³öK4[Fe(CN)6]Čܽā¶ČŠ”ÓŚNa4[Fe(CN)6]£¬ŃĒĢśĒč¼ŲæÉČÜÓŚĖ®£¬²»ČÜÓŚŅŅ“¼£¬Ņņ“ĖĻ“µÓ³ĮµķÓĆŅŅ“¼£»£Ø5£©øł¾ŻŠÅĻ¢£¬K++Fe3++ [Fe(CN)6]4££½KFe[Fe(CN)6]”ż£»£Ø6£©øł¾ŻCN-ŹŲŗć£¬n[K4[Fe(CN)6]]= ![]() mol=0.05mol£¬Ōņm[K4[Fe(CN)6]]= 0.05mol
mol=0.05mol£¬Ōņm[K4[Fe(CN)6]]= 0.05mol ![]() =18.4g£¬²śĀŹĪŖ£ŗ
=18.4g£¬²śĀŹĪŖ£ŗ ![]() ”Į100%=50%”£
”Į100%=50%”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æa-ĖÉÓĶ“¼æɾŅŌĻĀĀ·ĻßŗĻ³É£¬Š”·½æņÖŠµÄĆæŅ»×ÖÄøø÷“ś±ķŅ»ÖÖÓŠ»śĪļ£ŗ

æɹ©Ń”ŌńµÄŹŌ¼Į£ŗ¢ŁBr2¢ŚH2¢ŪO2
ĢįŹ¾£ŗ
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹŌ¼Į1ŹĒ______£¬ŹŌ¼Į2ŹĒ__________£ØĢīŠ“ŹŌ¼Į»ÆѧŹ½£©”£
£Ø2£©DµÄ½į¹¹¼ņŹ½ŹĒ_______£¬GµÄ½į¹¹¼ņŹ½ŹĒ_______”£
£Ø3£©a-ĖÉÓĶ“¼ŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘŹĒ__________£¬Fµ½HµÄ·“Ó¦ĄąŠĶŹĒ__________”£
£Ø4£©”°FµÄĶ¬·ÖŅģ¹¹ĢåÓŠ¶ąÖÖ, ĘäÖŠÓėFŗ¬ÓŠµÄ¹ŁÄÜĶŲ»Ķ¬ĒŅŗ¬ÓŠŅ»ÖÖ¹ŁÄÜĶŵÄÓŠ»śĪļÓŠ_____ÖÖ”£
£Ø5£©E×Ŗ»ÆĪŖFµÄ·“Ó¦·½³ĢŹ½ŹĒ________________”£
£Ø6£©½įŗĻĢāŹöŠÅĻ¢£¬ÓÉ1£¬3-¶”¶žĻ©”¢ŅŅ“¼ŗĻ³ÉŅ»ĀČ“ś»·¼ŗĶéµÄŗĻ³ÉĀ·ĻߣØĪŽ»śŹŌ¼ĮČĪŃ”£©: _____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĆܱÕČŻĘ÷ÖŠŅ»¶ØĮæ»ģŗĻĘųĢå·¢Éś·“Ó¦£ŗ2A(g)+B(g)![]() xC(g)£¬“ļµ½Ę½ŗāŹ±²āµĆAµÄÅضČĪŖ0.5mol/L£¬ŌŚĪĀ¶Č²»±äµÄĢõ¼žĻĀ£¬½«ČŻĘ÷ÖŠµÄČŻ»żĄ©“óµ½ŌĄ“2±¶£¬ŌŁ“ļĘ½ŗāŹ±£¬²āµĆAµÄÅضČĪŖ0.3mol/L£¬ĻĀĮŠÓŠ¹ŲÅŠ¶ĻÕżČ·µÄŹĒ
xC(g)£¬“ļµ½Ę½ŗāŹ±²āµĆAµÄÅضČĪŖ0.5mol/L£¬ŌŚĪĀ¶Č²»±äµÄĢõ¼žĻĀ£¬½«ČŻĘ÷ÖŠµÄČŻ»żĄ©“óµ½ŌĄ“2±¶£¬ŌŁ“ļĘ½ŗāŹ±£¬²āµĆAµÄÅضČĪŖ0.3mol/L£¬ĻĀĮŠÓŠ¹ŲÅŠ¶ĻÕżČ·µÄŹĒ
A. x=3 B. Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
C. BµÄ×Ŗ»ÆĀŹ½µµĶ D. CµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĮæµÄ»ģŗĻĘųĢåŌŚĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗxA(g)£«yB(g)![]() zC(g)£¬“ļµ½Ę½ŗāŗó²āµĆAĘųĢåµÄÅضČĪŖ0.5 mol”¤L£1£¬±£³ÖĪĀ¶Č²»±ä£¬½«ĆܱÕČŻĘ÷µÄČŻ»żŃ¹ĖõĪŖŌĄ“µÄŅ»°ėŌŁ“Ī“ļµ½Ę½ŗāŗ󣬲āµĆAÅضČĪŖ0.8 mol”¤L£1£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
zC(g)£¬“ļµ½Ę½ŗāŗó²āµĆAĘųĢåµÄÅضČĪŖ0.5 mol”¤L£1£¬±£³ÖĪĀ¶Č²»±ä£¬½«ĆܱÕČŻĘ÷µÄČŻ»żŃ¹ĖõĪŖŌĄ“µÄŅ»°ėŌŁ“Ī“ļµ½Ę½ŗāŗ󣬲āµĆAÅضČĪŖ0.8 mol”¤L£1£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ B. x+y£¼z
C. BµÄĪļÖŹµÄĮæÅØ¶Č¼õŠ” D. CµÄĢå»ż·ÖŹż½µµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ä»ÆŠčæĖ·žĻąĶ¬ĄąŠĶ×÷ÓĆĮ¦µÄŹĒ( )
A.µāŗĶøɱłµÄÉż»ŖB.¹čŗĶC60µÄČŪ»Æ
C.ĀČ»ÆĒāŗĶĀČ»ÆÄʵÄČܽāD.äåŗĶ¹ÆµÄĘų»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»Æѧ¼üŹĒŅ»ÖÖĻą»„×÷ÓĆ£¬Ėü“ęŌŚÓŚ( )
A. ·Ö×ÓÖ®¼äB. ĪļÖŹÖŠµÄŌ×ÓÖ®¼ä
C. ¹¹³ÉĪļÖŹµÄĖłÓŠĪ¢Į£Ö®¼äD. ·Ö×Ó»ņŌ×ÓĶÅÖŠĻąĮŚµÄŌ×ÓÖ®¼ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒijĪļÖŹ¼×µÄČܽā¶ČĒśĻߣ®Ēó£ŗ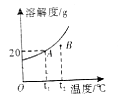
¢Łt1”ę£¬¼×µÄ±„ŗĶČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż£Ø¾«Č·µ½0.1%£©£»
¢Śt2”ę£¬Bµć¶ŌÓ¦µÄČÜŅŗŹĒ·ń±„ŗĶ£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚSO2µÄŠšŹöÕżČ·µÄŹĒ( )
A.SO2ŹĒ¾ßÓŠĘÆ°××÷ÓĆ£¬æÉŹ¹ŹÆČļĶŹÉ«B.SO2ÓėNaOHČÜŅŗ·“Ӧɜ³ÉNa2SO4
C.SO2ÄÜŹ¹äåĖ®ĶŹÉ«£¬ŹĒŅņĪŖSO2¾ßÓŠ»¹ŌŠŌD.SO2ÓŠ¶¾£¬²»ÄÜÓĆ×÷Ź³Ę·Ģķ¼Ó¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠĻĀĮŠŹ®ÖÖĪļÖŹ£ŗ¢ŁNa2O ¢ŚCu(OH)2 ¢ŪZn ¢ÜCaCO3 ¢ŻĮņĖįČÜŅŗ ¢ŽBa(OH)2 ¢ßøɱł ¢ąA12(SO4)3 ¢įHClĖ®ČÜŅŗ ¢āKHSO4
(1)ĘäÖŠŹōÓŚ·Ēµē½āÖŹµÄÓŠ_____________(ĢīŠņŗÅ)”£
(2)Ķł¢ŚÖŠ¼ÓČė¹żĮæµÄ0.1 mol/L¢āµÄĖ®ČÜŅŗ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ___________£¬ĻņĖłµĆČÜŅŗÖŠ¼ĢŠų¼ÓČė¢Ū£¬»į²śÉśĪŽÉ«ĘųÅŻ£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ_____________________”£
(3)ŗø½ÓĶĘ÷Ź±£¬æÉĻČÓĆNH4Cl³żČ„Ęä±ķĆęµÄŃõ»ÆĶŌŁ½ųŠŠŗø½Ó£¬øĆ·“Ó¦æɱķŹ¾ĪŖ£ŗ4CuO+2NH4Cl![]() 3Cu+CuCl2+N2”ü+4H2O
3Cu+CuCl2+N2ӟ+4H2O
¢ŁÓĆĖ«ĻßĒűźĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣______________________ ”£
¢ŚøĆ·“Ó¦ÖŠ£¬±»Ńõ»ÆµÄŌŖĖŲŹĒ £¬Ńõ»Æ¼ĮŹĒ__________________”£
¢Ū»¹Ō¼ĮÓėŃõ»Æ²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ_________________”£
¢Ü·“Ó¦ÖŠČō²śÉś0.2 molµÄµŖĘų£¬ŌņÓŠ_______________molµÄµē×Ó×ŖŅĘ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com