
| A. | CH2=CH2+Br2 | B. | CH2=CH-CH2-CH3+HCl | ||
| C. | CH3-CH=CH2+H2O | D. | nCH2=CH-CH3 |
分析 A.乙烯和溴发生加成反应生成1,2-二溴乙烷;
B.CH2=CH-CH2-CH3和HCl发生加成反应生成1-氯丁烷或2-氯丁烷;
C.丙烯和水发生加成反应生成1-丙醇或2-丙醇;
D.丙烯发生加聚反应生成聚丙烯.
解答 解:A.乙烯和溴发生加成反应生成1,2-二溴乙烷,只有一种产物,所以产物为纯净物,故A正确;
B.CH2=CH-CH2-CH3和HCl发生加成反应生成1-氯丁烷或2-氯丁烷,产物有两种,所以产物不是纯净物,故B错误;
C.丙烯和水发生加成反应生成1-丙醇或2-丙醇,产物有两种,所以产物不是纯净物,故C错误;
D.丙烯发生加聚反应生成聚丙烯,n不同产物不同,所以产物不是纯净物,故D错误;
故选A.
点评 本题以产物种类判断为载体考查有机物结构和性质,为高频考点,明确官能团及其性质关系、反应特点是解本题关键,侧重考查学生分析判断能力,易错选项是D,很多同学往往忽略化学式中n而导致错误.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入硫酸酸化的NaCl溶液,生成白色沉淀,证明原溶液中含Ag+ | |
| B. | 向溶液中加入稀盐酸,生成使澄清石灰水变浑浊的无色无味气体,则原溶液中含CO32- | |
| C. | 向溶液中加入硝酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中含SO42- | |
| D. | 溶液中加入HCl酸化后,再加入BaCl2溶液,有白色沉淀产生,则溶液中含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ③④ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(K+)+c(H+)=c(S2-)+c(HS-)+c(OH-) | B. | c(K+)+c(S2-)=0.3mol/L | ||
| C. | c(K+)=2[c(S2-)+c(HS-)+c(H2S)] | D. | c(OH-)=c(H+)+c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 用量筒量取浓硫酸时,俯视刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑤⑦⑥ | B. | ④⑥③⑦⑤⑥ | C. | ②⑥③⑦⑤⑥ | D. | ①⑥③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
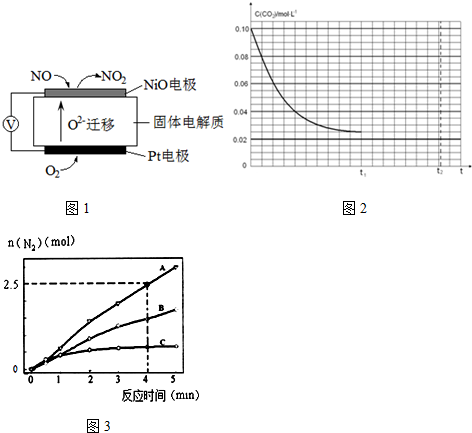
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
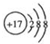 .
.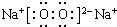 ,该产物所含有的化学键类型有离子键、非极性键.
,该产物所含有的化学键类型有离子键、非极性键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com