
| A. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| B. | 熔点由高到低:SiC>Si>SiO2>Ge | |
| C. | 沸点由高到低:NH3>PH3>AsH3>SbH3 | |
| D. | 晶格能由大到小:NaI>NaBr>NaCl>NaF |
分析 A.原子晶体中键长越短,共价键越强,硬度越大;
B.原子晶体中键长越短,共价键越强,熔沸点越高;
C.相对分子质量越大,分子晶体的沸点越高,氨气分子可形成氢键,沸点最高;
D.晶格能与离子半径成反比,与所带电荷成正比.
解答 解:A.由于原子半径C<Si,所以键长C-C<C-Si<Si-Si,键长越短,共价键越强,硬度越大,因此硬度:金刚石>碳化硅>晶体硅,故A正确;
B.由于原子半径Ge>Si>C>O,所以键长Ge-Ge>Si-Si>Si-C>Si-O,键长越短,共价键越强,熔沸点越高,所以熔点由高到低:SiO2>SiC>Si>Ge,故B错误;
C.相对分子质量越大,分子晶体的沸点越高,氨气分子可形成氢键,沸点最高,因此沸点由高到低:NH3>SbH3>AsH3>PH3,故C错误;
D.由于离子半径F-<Cl-<Br-<I-,所带电荷相同,所以晶格能为NaI<NaBr<NaCl<NaF,故D错误;
故选A.
点评 本题考查晶体熔沸点高低判断,侧重考查晶体类型判断及晶体熔沸点高低影响因素,注意晶格能、金属键与离子半径、离子所带电荷关系,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
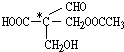 其中带*号的碳原子即是手性碳原子,现欲使该物质因不含手性碳原子而失去光学活性,下列反应中不可能实现的是( )
其中带*号的碳原子即是手性碳原子,现欲使该物质因不含手性碳原子而失去光学活性,下列反应中不可能实现的是( )| A. | 加成反应 | B. | 消去反应 | C. | 水解反应 | D. | 氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (I)、某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(I)、某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它位于周期表的第四周期、第ⅠA族 | |
| B. | 在钠、钾、铷三种单质中,相同条件下铷与水的反应速率最小 | |
| C. | 氢氧化铷是弱碱 | |
| D. | 硝酸铷是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
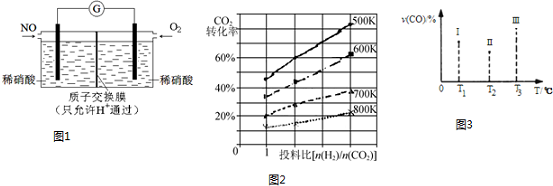
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜极为负极 | B. | 电子从铜沿导线转移到铁 | ||
| C. | 铁表面析出金属铜 | D. | 总反应为Fe+CuSO4=FeSO4+Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
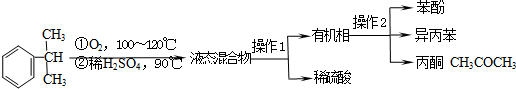
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精. | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水 和酒精等有机溶剂. | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机 杂质的试剂是①A.(填写右边字母) | A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯 酚的方案: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液,若试管中溶液颜色变为②紫色,则丙酮中含有苯酚,反之则没有. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com