



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、平衡向逆反应方向移动 |
| B、平衡不移动 |
| C、C的百分含量增大 |
| D、B的浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和浓溴水用铁作催化剂制溴苯 |
| B、向装有MnO2的烧瓶中滴加浓盐酸制Cl2 |
| C、淀粉与质量分数为20%的硫酸共煮制单糖 |
| D、电石与水反应在启普发生器中进行制乙块 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
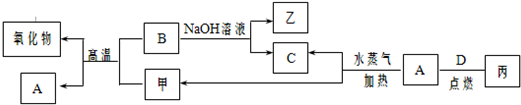
| 乙醇(乙酸) | 乙烯(二氧化硫) | 乙酸乙酯(乙醇) | |
| 加入试剂 | |||
| 分离方法 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 已知 2mol SO2(g)氧化为2mol SO3(g) 的能量变化如图1所示:
已知 2mol SO2(g)氧化为2mol SO3(g) 的能量变化如图1所示:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如右下图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如右下图所示装置.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中无硝酸亚铁 |
| B、反应前HNO3溶液的浓度为2.0mol?L-1 |
| C、反应后溶液中c(NO3-)=1.6mol?L-1 |
| D、反应后的溶液最多还能溶解1.61g Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com