


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源: 题型:
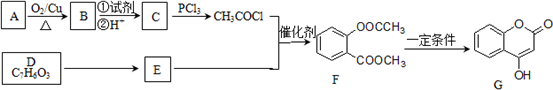
| PCl3 |
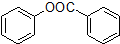 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
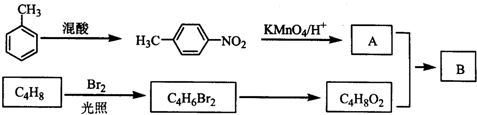
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验中使用的主要仪器是分液漏斗 |
| B、溴在四氯化碳中的溶解度比在水中的溶解度大 |
| C、不可把萃取剂四氯化碳换成酒精 |
| D、分液时,水从分液漏斗下口流出,溴的四氯化碳溶液从分液漏斗上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
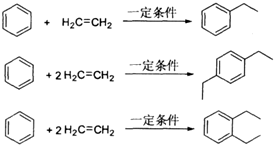
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、CuSO4?5H2O、纯碱 |
| B、硫酸氢钠、空气、纯碱 |
| C、氧化铁、明矾、熟石灰 |
| D、硝酸、食盐水、烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在一定浓度的氯水中加小苏打有气泡生成 |
| B、新制氯水中只存在2个平衡状态 |
| C、氯水应保存在棕色瓶中,久置的氯水,PH值减小 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com