

分析 (C2H4)n为聚乙烯,乙烯发生加聚反应生成聚乙烯,则A为CH2=CH2,乙烯和H2O发生加成反应生成乙醇,乙醇结构简式为CH3CH2OH,乙醇在Cu作催化剂、加热条件下发生氧化反应生成C,C为CH3CHO,乙醛被催化氧化生成D,D为CH3COOH,在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,则C4H8O2为乙酸乙酯,结构简式为CH3COOCH2CH3,据此分析解答.
解答 解:(C2H4)n为聚乙烯,乙烯发生加聚反应生成聚乙烯,则A为CH2=CH2,乙烯和H2O发生加成反应生成乙醇,乙醇结构简式为CH3CH2OH,乙醇在Cu作催化剂、加热条件下发生氧化反应生成C,C为CH3CHO,乙醛被催化氧化生成D,D为CH3COOH,在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,则C4H8O2为乙酸乙酯,结构简式为CH3COOCH2CH3,
(1)通过以上分析知,乙醇结构简式为CH3CH2OH,故答案为:CH3CH2OH;
(2)通过以上分析知,反应①②③④属于氧化反应的是③,故答案为:③;
(3)反应④为乙醇和乙酸的酯化反应,该反应的化学方程式是CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(4)(C2H4)n的链节是为-CH2CH2-,故答案为:-CH2CH2-.
点评 本题考查有机物推断,为高频考点,涉及烯烃、醇、醛、羧酸、酯之间的转化,明确常见反应类型、反应条件及常见有机物官能团及其性质关系即可解答,知道高聚物链节及单体的判断方法,题目难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
 分别与足量Na、NaOH水溶液、H2反应,试剂最大用量正确的是( )
分别与足量Na、NaOH水溶液、H2反应,试剂最大用量正确的是( )| Na | NaOH | H2 | |
| A | 1mol | 1mol | 3mol |
| B | 2mol | 2mol | 5mol |
| C | 1mol | 3mol | 4mol |
| D | 1mol | 3mol | 5mol |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
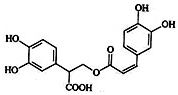 迷迭香酸是从蜂花属植物中提取得到的酸性物质.其结构如图.
迷迭香酸是从蜂花属植物中提取得到的酸性物质.其结构如图. | A. | 迷迭香酸属于芳香烃 | |
| B. | 1mol迷迭香酸最多能和9mol氢气发生加成反应 | |
| C. | 迷迭香酸可以发生加成反应、取代反应和酯化反应 | |
| D. | 迷迭香酸的化学式为C18H18O8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
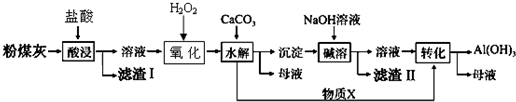
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 工作时,电解质溶液中K+向负极移动 | |
| B. | 电路若有0.4mol电子通过,则消耗O2的量为0.2mol | |
| C. | 一段时间后溶液中OH-浓度将升高 | |
| D. | 正极反应式为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱的化学式:NaHCO3 | B. | Cl原子的结构示意图: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 质量数为37的氯原子:${\;}_{17}^{37}$Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com