
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:0110 模拟题 题型:填空题
 CO(g)+2H2(g);△H=-36kJ/mol……… ①
CO(g)+2H2(g);△H=-36kJ/mol……… ①  CO(g)+3H2(g);△H=+216kJ/mol………②
CO(g)+3H2(g);△H=+216kJ/mol………②  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为______________。
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为______________。 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①; 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;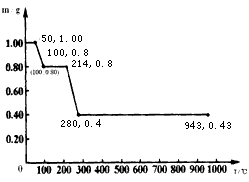
查看答案和解析>>
科目:高中化学 来源:0110 模拟题 题型:填空题
 CO(g)+2H2(g);△H= -36kJ/mol ①
CO(g)+2H2(g);△H= -36kJ/mol ①  CO(g)+3H2(g);△H= +216kJ/mol ②
CO(g)+3H2(g);△H= +216kJ/mol ②  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。 Na2FeO2+H2O+NH3↑ ①;
Na2FeO2+H2O+NH3↑ ①; 4Na2Fe2O4+3NH3↑ ②;
4Na2Fe2O4+3NH3↑ ②;
查看答案和解析>>
科目:高中化学 来源:2007-2008学年天津五中高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com