
反应N2+3H 2NH3,正反应的反应速率为v1,逆反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为( )
2NH3,正反应的反应速率为v1,逆反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大 B.同时减小 C.v1增大,v2减小 D.v1减小,v2增大
科目:高中化学 来源:2015-2016学年广东省高二下期中化学试卷(解析版) 题型:选择题
将①中溶液逐滴滴入②中,预测的现象与实际相符的是( )
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 |
C. | 氯化铁溶液 | 苯酚水溶液 | 溶液变成紫色 |
D. | 氨水 | 氯化铝溶液 | 立即生成白色沉淀,最终沉淀逐渐溶解 |
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是

A.该弱酸在滴定前的浓度大于0.001mol/L
B.由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(Na+) >c(A-) > c(OH-) >c(H+)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列事实不能用元素周期律解释的是
A.向Na2SO3溶液中加盐酸,有气泡产生
B.0.1 mol·L-1溶液的pH:NaOH > LiOH
C.Mg、Al与同浓度盐酸反应,Mg更剧烈
D.气态氢化物的稳定性:HBr > HI
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N(g)+3H2(g) 2NH3(g),在20℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是()
2NH3(g),在20℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是()

A.点a的正反应速率比b 的小
B.点c处反应达到平衡
C.点d(t2时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,该反应在25℃下反应达到平衡状态,所用的时间比原来的少
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
法国科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性 B.该粒子质量数为4
C.在周期表中与氢元素占同一位置 D.该粒子质量比氢原子大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:填空题
(1)某城市下了一场酸雨,经检验,酸雨中除H+以外,还含有Na+、Cl-、NH4+、SO42—等离子,其浓度如下表所示:
离子 | Na+ | Cl- | NH4+ | SO42— |
浓度(mol·L-1) | 7.0×10-6 | 3.5×10-5 | 2.3×10-5 | 2.5×10-6 |
该酸雨的c(H+)=________。
(2)元素周期表是学习和研究化学的重要工具,下图是元素周期表的一部分
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | A | 2He | ||||||
2 | B | C | D | |||||
3 | E | F | G | H | I | J | K | L |
①表中G的元素符号是 ;最易获得电子的元素是 (填名称)。
②下列有关元素性质的递变规律正确的是
A.氢氧化物的碱性E<F<G B.获得电子的能力I>J>K
C.气态氢化物的稳定性D>K D.原子半径H<I<J<K
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
有一瓶无色气体可能含有CO2、HBr、NO2、HCl、SO2中的一种或几种。将此气体通入足量稀氯水中,恰好完全反应,得无色透明溶液,把此溶液分成两份,分别加入盐酸酸化了的BaCl2溶液和硝酸酸化了的AgNO3溶液,均出现白色沉淀,以下结论正确的是
A.不能确定原气体中是否含有SO2
B.原气体中肯定有HCl
C.原气体中肯定没有CO2
D.原气体中肯定没有HBr、NO2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:选择题
向甲、乙两个容积均为1L的恒容容器中,分别充入2 molA、2 mol B和1 molA、1 molB。相同温度下.发生反应:A(g)+B(g)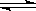 xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示。下列说法正确的是
xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示。下列说法正确的是

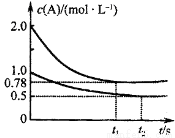
A.甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙)
B.x不可能等于2
C.将乙容器升温可使甲、乙容器内各物质的体积分数相同
D.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol/L<c(A)<1.56 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com