
| 编号 | 化学反应 | 离子方程式 | 评 价 |
| A | 碳酸钙与 醋酸反应 | CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解 质,不应写成离子形式 |
| B | 苯酚钠溶液中 通入CO2 | 2C6H5O-+CO2+H2O→2C6H5OH+CO32- | 正确 |
| C | NaHCO3的水解 | HCO3-+H2O=CO32-+H3O+ | 错误,水解方程式 误写成电离方程式 |
| D | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 错误,离子方程式中 Fe2+与Br-的物质的量 之比与化学式不符 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碳酸钙在离子反应中保留化学式,碳酸钙为强电解质;
B.反应生成苯酚和碳酸氢钠;
C.水解生成碳酸和氢氧根离子,电离生成碳酸根离子和氢离子;
D.等物质的量反应,由电子守恒可知亚铁离子全部被氧化,溴离子一半被氧化.
解答 解:A.碳酸钙与醋酸反应的离子反应为CaCO3+2CH3COOH=Ca2++CO2↑+H2O+2CH3COO-,碳酸钙为强电解质,评价不合理,故A错误;
B.苯酚钠溶液中通入CO2的离子反应为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故B错误;
C.NaHCO3的水解为HCO3-+H2O=H2CO3+OH-,电离为HCO3-+H2O=CO32-+H3O+,故C正确;
D.等物质的量的FeBr2和Cl2反应的离子反应为2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,评价不合理,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| B. | 2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | Mg2++H++2SO42-+2Ba2++3OH-=Mg(OH)2↓+2BaSO4↓+H2O | |
| D. | 3Mg2++2H++4SO42-+4Ba2++8OH-=3Mg(OH)2↓+4BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 实验操作 | 实验目的 |
| ① | 将足量的SO2气体通入装有品红溶液的试管中 | 研究SO2具有漂白性 |
| ② | 向盛有10molAgNO3溶液的试管中滴加几滴NaCl溶液,再向其中滴加几滴Na2S | 比较Ksp(AgCl)与Ksp(Ag2S)的大小 |
| ③ | 测定等物质的量浓度HCl,HNO3的pH | 比较Cl,N的非金属性强弱 |
| ④ | 向2支试管中加入同体积通浓度的H2C2O4溶液,再分别加入同体积不同浓度的酸性KMnO4 | 研究浓度对反应速率的影响 |
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
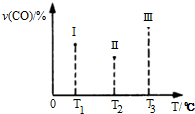 能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义.
能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义.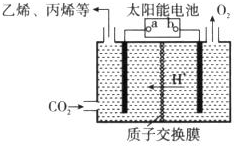
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,饱和CaCO3溶液与饱和CaF2溶液等体积混合,不会析出CaF2固体 | |
| B. | 25℃时,饱和CaCO3溶液与饱和CaF2溶液相比,前者Ca2+浓度大 | |
| C. | 25℃时,在CaCO3悬浊液中加人NaF固体,CaCO3全部溶解 | |
| D. | 25℃时,CaCO3固体在盐酸中的Ksp比在氨水中的Ksp大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向SO2水溶液中加入少量NaHCO3粉末,有气泡产生,说明SO2水溶液呈酸性 | |
| B. | 向SO2水溶液中滴加Ba(NO3)2溶液,有白色沉淀产生,说明SO2水溶液中含有SO42- | |
| C. | 将SO2水溶液中通入H2S气体,有淡黄色沉淀产生,说明SO2水溶液具有氧化性 | |
| D. | 向KMnO4溶液中滴加SO2水溶液,溶液颜色褪去,说明SO2水溶液具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用装置A完成SiCl4的制备 | |
| B. | 用装置B进行蒸馏提纯SiCl4 | |
| C. | 用装置C进行滴定达终点时现象是:锥形瓶内溶液变为紫红色且半分钟内不变色 | |
| D. | 配制0.1 mol•L-1KMnO4溶液定容摇匀后,发现液面低于刻度线,加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com