
| 共价键 | C-C | C=C | C≡C |
| 键长(nm) | 0.154 | 0.134 | 0.120 |
| 键能(kJ/mol) | 347 | 612 | 838 |
| A. | 0.154 nm>苯中碳碳键键长>0.134nm | |
| B. | C=O键键能>C-O键键能 | |
| C. | 乙烯的沸点高于乙烷 | |
| D. | 烯烃比炔烃更易与溴加成 |
分析 A.苯中的化学键键长介于碳碳单键与碳碳双键之间;
B.单键的键能小于双键的键能;
C.乙烯的沸点低于乙烷;
D.双键键能小于三键,更易断裂.
解答 解:A.苯中的化学键键长介于碳碳单键与碳碳双键之间,所以0.154 nm>苯中碳碳键键长>0.134nm,故A正确;
B.单键的键能小于双键的键能,则C=O键键能>C-O键键能,故B正确;
C.乙烷的相对分子质量大于乙烯,则乙烷的沸点高于乙烯,故C错误;
D.双键键能小于三键,更易断裂,所以乙烯更易发生加成反应,则烯烃比炔烃更易与溴加成,故D正确.
故选C.
点评 本题考查了有机物的结构与性质、化学键,题目难度不大,侧重于基础知识的考查,注意对基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
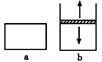
| A. | x的值为2 | |
| B. | B物质可为固体或液体 | |
| C. | 平衡时,a容器的体积小于V L | |
| D. | a、b容器中从起始到平衡所需时间相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
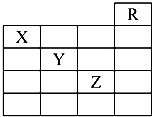 如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | 用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.0 | B. | 1.35 | C. | 1.5 | D. | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
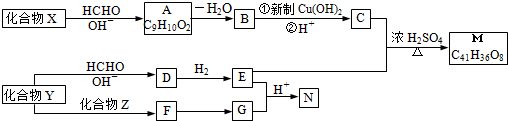
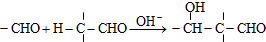
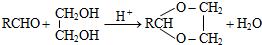
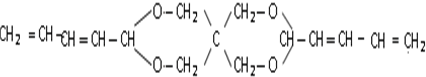
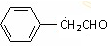 Z:CH2=CHCHO E:
Z:CH2=CHCHO E: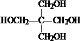
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com