
【题目】下列关于钠的氧化物的叙述正确的是( )
A. Na2O2是白色固体,和冷水反应得到O2和NaOH
B. Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水
C. Na2O不稳定,能继续被O2氧化生成Na2O2
D. 都能与酸反应生成含氧酸盐,都是碱性氧化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I﹣=2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI﹣淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )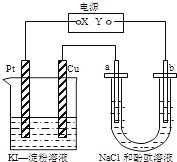
A.若a极变红,则在Pt电极上:2I﹣﹣2e﹣=I2 淀粉遇碘变蓝
B.若b极变红,在Pt电极上:4OH﹣﹣4e﹣=2H2O+O2 O2将I﹣氧化为I2 , 淀粉遇碘变蓝
C.若a极变红,在Cu电极上:开始Cu+I﹣﹣e﹣=CuI,一段时间后2I﹣﹣2e﹣═I2 淀粉遇碘变蓝
D.若b极变红,在Cu极上:Cu﹣2e﹣═Cu2+ Cu2+ 显蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3和NaHCO3性质的说法正确的是( )
A.热稳定性:Na2CO3>NaHCO3
B.相同温度时的水溶性:Na2CO3<NaHCO3
C.等物质的量浓度的溶液的碱性:Na2CO3<NaHCO3
D.与同浓度的盐酸反应的剧烈程度:Na2CO3>NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对室温下100mL pH=2的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( ) 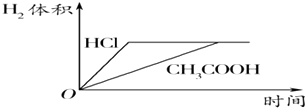
A.加水稀释至溶液体积为200mL,醋酸溶液的pH变为4
B.温度都升高20°C后,两溶液的pH不再相等
C.加水稀释至溶液体积为200mL后,两种溶液中c(OH﹣)都减小
D.加足量的锌充分反应后,两溶液中产生的氢气体积可用上图表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用甘蔗渣合成某重要化合物X(化学式为C11H18O4)的一种路线如图: 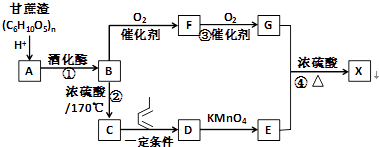
已知信息: ![]()
回答下列问题:
(1)D的结构简式为 , F官能团的名称为 ,
(2)②的反应类型为 , ③的反应类型为 .
(3)①的化学方程式为 . ④的化学方程式为 .
(4)检验甘蔗渣在酸性条件下水解后有A生成的试剂是 .
(5)写出满足下列条件的D的所有同分异构体的结构简式:Ⅰ.含六元环
(6)根据本题信息,以乙炔、丁二烯为主要有机原料,通过两步反应制备 ![]() 的合成路线为 .
的合成路线为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物([Cr(CH3COO)2)]22H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下: 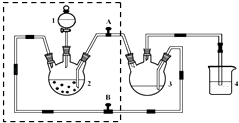
Zn(s)+2HCl(aq)=ZnCl2(aq)+H2(g); 2CrCl3(aq)+Zn(s)=2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO﹣(aq)+2H2O(l)=[Cr(CH3COO)2]22H2O (s)
请回答下列问题:
(1)检查虚框内装置气密性的方法是 .
(2)本实验中所有配制溶液的水需煮沸,其原因是 . 装置4的作用是 .
(3)将生成的CrCl2溶液与CH3COONa溶液混合时的操作是阀门A、阀门B (填“打开”或“关闭”).
(4)本实验中锌粒须过量,其原因是 .
(5)为洗涤[Cr(CH3COO)2)]22H2O产品,下列方法中最适合的是 .
A.先用盐酸洗,后用冷水洗
B.先用冷水洗,后用乙醇洗
C.先用冷水洗,后用乙醚洗
D.先用乙醇洗涤,后用乙醚洗
(6)下列对产物进一步处理不正确的是 .
A.产物可用采用减压过滤得到晶体
B.在合适的温度下在烘箱内烘干
C.在温室下隔绝空气使其干燥
D.产物需要密封保存.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用以下装置制备并检验Cl2的性质.下列说法正确的是( ) 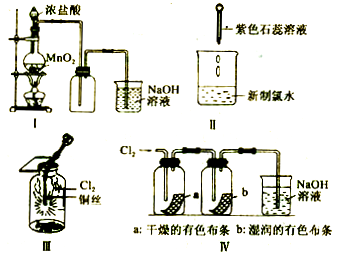
A.Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B.Ⅱ图:证明新制氯水具有酸性
C.Ⅲ图:产生了棕黄色的雾
D.Ⅳ图:湿润的有色布条褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+F2(g)═2HF(g) 的能量变化如图所示,下列有关叙述中正确的是( ) 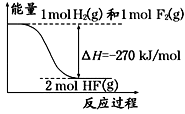
A.氟化氢气体分解生成氢气和氟气的反应是放热反应
B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D.断裂1 mol H﹣H键和1 mol F﹣F 键放出的能量大于形成2 mol H﹣F键放出的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com