
0.1 LijĘųĢ¬ĢžĶźČ«Č¼ÉÕ£¬ŌŚĻąĶ¬Ģõ¼žĻĀ²āµĆÉś³É0.1 L CO2ŗĶ0.2 LĖ®ÕōĘų”£øĆĢžµÄ·Ö×ÓŹ½ŹĒ(””””)
A£®CH4”” B£®C2H4
C£®C2H2 D£®C3H6
 æŚĖćÄÜŹÖĻµĮŠ“š°ø
æŚĖćÄÜŹÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
æĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚŃŠ¾æ³£ĪĀ”¢³£Ń¹ĻĀ”°ČĖ¹¤¹ĢµŖ”±µÄŠĀ·½·Ø”£ŌųÓŠŹµŃé±ØµĄ£ŗŌŚ³£ĪĀ”¢³£Ń¹”¢¹āÕÕĢõ¼žĻĀ£¬N2ŌŚ“߻ƼĮ(²ōÓŠÉŁĮæFe2O3µÄTiO2)±ķĆęÓėĖ®·¢Éś·“Ó¦£¬Éś³ÉµÄÖ÷ŅŖ²śĪļĪŖNH3”£½ųŅ»²½ŃŠ¾æNH3Éś³ÉĮæÓėĪĀ¶ČµÄ¹ŲĻµ£¬²æ·ÖŹµŃ鏿¾Ż¼ūĻĀ±ķ(¹āÕÕ”¢N2Ń¹Į¦1.0”Į105 Pa”¢·“Ó¦Ź±¼ä3 h)£ŗ
| T/K | 303 | 313 | 323 | 353 |
| NH3Éś³ÉĮæ/(10£6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
ĻąÓ¦µÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
N2(g)£«3H2O(l)===2NH3(g)£«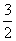 O2(g)
O2(g)
¦¤H£½765.2 kJ”¤mol£1
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Ēė»³öÉĻŹö·“Ó¦ŌŚÓŠ“߻ƼĮÓėĪŽ“߻ƼĮĮ½ÖÖĒéæöĻĀ·“Ó¦¹ż³ĢÖŠĢåĻµÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬²¢½ųŠŠ±ŲŅŖ±ź×¢”£
(2)ÓėÄæĒ°¹ć·ŗŹ¹ÓĆµÄ¹¤ŅµŗĻ³É°±·½·ØĻą±Č£¬øĆ·½·ØÖŠ¹ĢµŖ·“Ó¦ĖŁĀŹĀż”£ĒėĢį³öæÉĢįøßĘä·“Ó¦ĖŁĀŹĒŅŌö“óNH3Éś³ÉĮæµÄ½ØŅé£ŗ
________________________________________________________________________
________________________________________________________________________ӣ
(3)¹¤ŅµŗĻ³É°±µÄ·“Ó¦ĪŖN2(g)£«3H2(g)
 2NH3(g)”£ÉčŌŚČŻ»żĪŖ2.0 LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.60 mol N2(g)ŗĶ1.60 mol H2(g)£¬·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬NH3µÄĪļÖŹµÄĮæ·ÖŹż(NH3µÄĪļÖŹµÄĮæÓė·“Ó¦ĢåĻµÖŠ×ܵÄĪļÖŹµÄĮæÖ®±Č)ĪŖ
2NH3(g)”£ÉčŌŚČŻ»żĪŖ2.0 LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.60 mol N2(g)ŗĶ1.60 mol H2(g)£¬·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬NH3µÄĪļÖŹµÄĮæ·ÖŹż(NH3µÄĪļÖŹµÄĮæÓė·“Ó¦ĢåĻµÖŠ×ܵÄĪļÖŹµÄĮæÖ®±Č)ĪŖ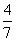 ”£¼ĘĖć£ŗ
”£¼ĘĖć£ŗ
¢ŁøĆĢõ¼žĻĀN2µÄĘ½ŗā×Ŗ»ÆĀŹ£»
¢ŚøĆĢõ¼žĻĀ·“Ó¦2NH3(g)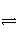
 N2(g)£«3H2(g)µÄĘ½ŗā³£Źż”£
N2(g)£«3H2(g)µÄĘ½ŗā³£Źż”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Īų£ØSe£©ŹĒČĖĢå±ŲŠčµÄĪ¢ĮæŌŖĖŲ£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĻĀĶ¼”£ĻĀĮŠ¹ŲÓŚĪųŌŖĖŲµÄŠšŹöÕżČ·µÄŹĒ
A. ĪųĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµŚĖÄÖÜĘŚµŚIVA×å
B. ĪųµÄ·Ē½šŹōŠŌ±ČSČõ
C. H2Se±ČHBrĪȶØ
D. ×īøß¼ŪŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖSeO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠ8ÖÖĪļÖŹ£ŗ¢Ł¼×Ķé””¢Ś±½””¢Ū¾ŪŅŅĻ©””¢Ü¾ŪŅģĪģ¶žĻ©””¢Ż2¶”Č²””¢Ž»·¼ŗĶé””¢ßĮŚ¶ž¼×±½””¢ą»·¼ŗĻ©£¬¼ČÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶĖÉ«£¬ÓÖÄÜÓėäåĖ®·“Ó¦Ź¹Ö®ĶĖÉ«µÄŹĒ(””””)
A£®¢Ū¢Ü¢Ż¢ą B£®¢Ü¢Ż¢ß¢ą
C£®¢Ü¢Ż¢ą D£®¢Ū¢Ü¢Ż¢ß¢ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¶ŌÓŚ±½ŅŅĻ©(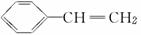 )µÄĻĀĮŠŠšŹö£ŗ¢ŁÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶĖÉ«£»¢ŚæÉ·¢Éś¼Ó¾Ū·“Ó¦£»¢ŪæÉČÜÓŚĖ®£»¢ÜæÉČÜÓŚ±½£»¢ŻÄÜÓėÅØĻõĖį·¢ÉśČ”“śÓ¦£»¢ŽĖłÓŠµÄŌ×ÓæÉÄܹ²Ę½Ćę£¬ĘäÖŠÕżČ·µÄŹĒ(””””)
)µÄĻĀĮŠŠšŹö£ŗ¢ŁÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶĖÉ«£»¢ŚæÉ·¢Éś¼Ó¾Ū·“Ó¦£»¢ŪæÉČÜÓŚĖ®£»¢ÜæÉČÜÓŚ±½£»¢ŻÄÜÓėÅØĻõĖį·¢ÉśČ”“śÓ¦£»¢ŽĖłÓŠµÄŌ×ÓæÉÄܹ²Ę½Ćę£¬ĘäÖŠÕżČ·µÄŹĒ(””””)
A£®¢Ł¢Ś¢Ü¢Ż B£®¢Ł¢Ś¢Ż¢Ž
C£®¢Ł¢Ś¢Ü¢Ż¢Ž D£®Č«²æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆ·ÖŅŗĀ©¶·æÉŅŌ·ÖĄėµÄŅ»×éŅŗĢå»ģŗĻĪļŹĒ
A£®äåŗĶ±½ B£®±½ŗĶäå±½ C£®Ė®ŗĶĻõ»ł±½ D£®±½ŗĶĘūÓĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

 ŅŃÖŖ£ŗxA£Øg£©+yB£Øg£© zC£Øg£©£»”÷H=a”£½«x molAŗĶy molB»ģŗĻŌŚĆܱÕČŻĘ÷ÖŠ£¬ŌŚ²»Ķ¬ĪĀ¶Č£ØT1>T2£©¼°Ń¹Ēæ£ØP1>P2£©ĻĀ£¬CµÄĪļÖŹµÄĮæn£ØC£©
ŅŃÖŖ£ŗxA£Øg£©+yB£Øg£© zC£Øg£©£»”÷H=a”£½«x molAŗĶy molB»ģŗĻŌŚĆܱÕČŻĘ÷ÖŠ£¬ŌŚ²»Ķ¬ĪĀ¶Č£ØT1>T2£©¼°Ń¹Ēæ£ØP1>P2£©ĻĀ£¬CµÄĪļÖŹµÄĮæn£ØC£©
Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
A£®x+y=z£»a>0 B£®x+y>z£»a<0
C£®x+y<z£»a<0 D£®x+y<z£»a>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠ·“Ó¦£ŗmA(g)+nB(g) pC(g)£¬“ļµ½Ę½ŗāŗ󣬵±ÉżøßĪĀ¶ČŹ±£¬BµÄ×Ŗ»ÆĀŹ±ä“ó£»µ±¼õŠ”Ń¹ĒæŹ±£¬»ģŗĻĢåĻµÖŠCµÄÖŹĮæ·ÖŹżŅ²¼õŠ”£¬Ōņ:
pC(g)£¬“ļµ½Ę½ŗāŗ󣬵±ÉżøßĪĀ¶ČŹ±£¬BµÄ×Ŗ»ÆĀŹ±ä“ó£»µ±¼õŠ”Ń¹ĒæŹ±£¬»ģŗĻĢåĻµÖŠCµÄÖŹĮæ·ÖŹżŅ²¼õŠ”£¬Ōņ:
(1)øĆ·“Ó¦µÄÄę·“Ó¦ĪŖ_________ČČ·“Ó¦£¬ĒŅm+n_________p(Ģī”°£¾”±”°=”±”°£¼”±)”£
(2)¼õŃ¹Ź±£¬AµÄÖŹĮæ·ÖŹż_________”£(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£¬ĻĀĶ¬)
(3)Čō¼ÓČėB(Ģå»ż²»±ä)£¬ŌņAµÄ×Ŗ»ÆĀŹ_________£¬BµÄ×Ŗ»ÆĀŹ_________”£
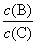 (4)ČōÉżøßĪĀ¶Č£¬ŌņĘ½ŗāŹ±B”¢CµÄÅضČÖ®±Č ½«_________”£
(4)ČōÉżøßĪĀ¶Č£¬ŌņĘ½ŗāŹ±B”¢CµÄÅضČÖ®±Č ½«_________”£
(5)Čō¼ÓČė“߻ƼĮ£¬Ę½ŗāŹ±ĘųĢå»ģŗĻĪļµÄ×ÜĪļÖŹµÄĮæ_________”£
(6)ČōBŹĒÓŠÉ«ĪļÖŹ£¬A”¢C¾łĪŽÉ«£¬Ōņ¼ÓČėC(Ģå»ż²»±ä)Ź±»ģŗĻĪļŃÕÉ«_______£¬¶ųĪ¬³ÖČŻĘ÷ÄŚŃ¹Ēæ²»±ä£¬³äČėÄŹĘųŹ±£¬»ģŗĻĪļŃÕÉ«_______(Ģī”°±äÉī”±”°±äĒ³”±»ņ”°²»±ä”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ė®µÄµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£ŗ
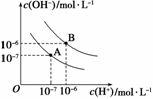
(1)ČōŅŌAµć±ķŹ¾25”ꏱĖ®µēĄėĘ½ŗāŹ±µÄĄė×ÓÅØ¶Č£¬µ±ĪĀ¶ČÉĻÉżµ½100”ꏱ£¬Ė®µÄµēĄėĘ½ŗāדĢ¬µ½Bµć£¬Ōņ“ĖŹ±Ė®µÄĄė×Ó»ż“Ó________Ōö¼Óµ½________”£
(2)½«pH£½8µÄĒāŃõ»Æ±µČÜŅŗÓėpH£½5µÄŃĪĖįČÜŅŗ»ģŗĻ²¢±£³Ö100”ęŗćĪĀ£¬ÓūŹ¹»ģŗĻČÜŅŗµÄpH£½7£¬ŌņĒāŃõ»Æ±µČÜŅŗÓėŃĪĖįµÄĢå»ż±ČĪŖ________”£
(3)ŅŃÖŖAnBmµÄĄė×Ó»żK£½[c(Am£«)]n”¤[c(Bn£)]m£¬Ź½ÖŠc(Am£«)ŗĶc(Bn£)±ķŹ¾Ąė×ÓµÄĪļÖŹµÄĮæÅØ¶Č”£ŌŚÄ³ĪĀ¶ČĻĀ£¬ĒāŃõ»ÆøĘČܽā¶ČĪŖ0.74 g£¬Ę䱄ŗĶČÜŅŗĆܶČÉčĪŖ1 g”¤cm£3£¬ĘäĄė×Ó»żĪŖK£½________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com