
| A.韧性比生铁好 | B.在冷的浓硫酸中钝化 |
| C.不能与盐酸反应 | D.在冷的浓硝酸中钝化泛使用 |
科目:高中化学 来源:不详 题型:单选题
| A.4 mol·L—1 | B.3 mol·L—1 | C.2 mol·L—1 | D.1 mol·L—1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 g | B.11.2 g | C.22.4 g | D.33.6 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:4 | B.2:1 | C.4:1 | D.3:4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2∶3 | B.3∶2 | C.1∶2 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
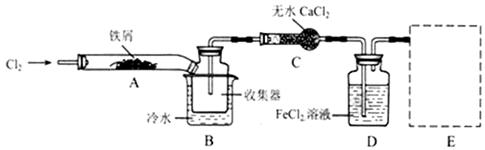
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| ①取少量所得溶液于试管中,加入少量KSCN溶液。 | _________________。 | 说明:假设②不成立,假设①或③成立;反应的离子方程式是_____________。 |
| ②另取少量所得溶液于试管中,加入少量酸性 KMnO4溶液。 | 溶液紫红色退去 | 说明:________________________。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
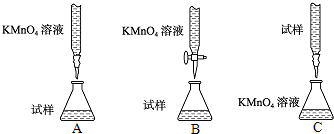

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com