
| A、X的原子半径大于Y的原子半径 |
| B、由X.Y组成的离子化合物中阴离子核外有18个电子 |
| C、X2Y可能是离子化合物,也可能是共价化合物 |
| D、由X.Y组成的化合物,溶于水后溶液呈碱性 |


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
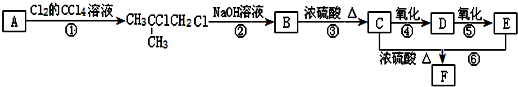
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气体使湿润的酚酞试液变红 |
| B、气体能使湿润的红色石蕊试纸变蓝 |
| C、气体与蘸有浓H2SO4的玻璃棒靠近 |
| D、气体与蘸有浓盐酸的玻璃棒靠近 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含Na+为2mol的Na2SO4溶液 |
| B、将31g Na2O溶于水并配成1L的溶液 |
| C、将0.5mol/L的KNO3溶液100mL加热蒸发掉50g水的溶液 |
| D、将58.5gNaCl溶于1L水所得的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 用二氧化氯、铁酸钠(Na2FeO4)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术,ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯、铁酸钠(Na2FeO4)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术,ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com