
【题目】如图所示原电池装置,回答下列问题:
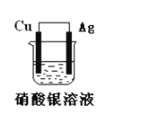
(1)此电池的负极是:______,正极的电极反应式是:________。
(2)该电池工作一段时间后,装置中出现的现象________,将银电极小心取出洗涤并晾干,经称量发现比原来增重了5.4g。则导线中通过的电子的物质的量为 ________。
【答案】铜或Cu Ag+ +e- =Ag 铜电极变细,银电极变粗,溶液颜色变蓝 0.05mol
【解析】
(1)Cu比Ag活泼,做原电池的负极,原电池中负极发生氧化反应,正极发生还原反应;
(2)根据正负极上发生的反应以及电解质溶液的浓度变化判断反应现象,根据电极反应式计算通过电子的物质的量。
(1)Cu比Ag活泼,做原电池的负极,Ag为原电池的正极,发生还原反应,电极反应为Ag++e-=Ag,
故答案为:铜或Cu,Ag++e-=Ag。
(2)原电池工作时,负极铜失去电子被氧化生成铜离子,铜的质量逐渐减少,银极上生成银,质量逐渐增大,溶液中生成铜离子,溶液颜色变蓝,当银电极质量增加5.4g,则n(Ag)=![]() =0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol。
=0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol。
故答案为:铜电极变细,银电极变粗,溶液颜色变蓝;0.05mol。


科目:高中化学 来源: 题型:
【题目】一定量的H2和Cl2充分燃烧后,将反应生成的气体通入100mL1.0mol/L的NaOH溶液中,两者恰好完全反应,生成NaClO为0.01mol。则燃烧前H2和Cl2的物质的量之比为
A. 5:4 B. 4:5 C. 4:3 D. 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低合金高强度钢是支撑"鸟巢"的铁骨钢筋,除含有铁元素外,还含有Mn(锰),Ti(钛),(铬),(铌)等合金元素,下列有关说法正确的是( )
A. Fe位于元素周期表的第四周期,第VIIIB族
B. 46TiO、 48TiO、50TiO互为同位素
C. Mn 2O7是酸性氧化物
D. ![]() 原子核内有个51个中子,核外有 41个电子
原子核内有个51个中子,核外有 41个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯(![]() )是合成橡胶和塑料的重要单体,也是生产某些药物、农药的中间体。化合物E是一种昆虫信息素,可以通过以下流程制备。
)是合成橡胶和塑料的重要单体,也是生产某些药物、农药的中间体。化合物E是一种昆虫信息素,可以通过以下流程制备。

完成下列填空:
(1)反应②的反应类型__________;上述流程中的物质,与B互为同分异构体是__________。写出B的属于芳香烃的一种同分异构体的结构简式__________,该物质的名称为_________。
(2)反应①中,A和苯按摩尔比1:1完全反应,产物只有B。写出A的结构简式___________。
(3)写出反应③的化学方程式____________________________________。
(4)以B为原料制取C的反应是可逆反应,分离C、B混合物的实验操作为____________。
(5)苯乙烯露置于空气中可被氧化为苯甲醛和甲醛。设计实验方案检验苯乙烯样品是否被氧化变质______________________________________。
(6)参照上述合成路线的表示方法,设计以苯乙烯为原料经过三步反应制备新型高分子导电材料PPA(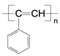 )的合成路线,并注明必要的反应条件。(无机物任选)_____________
)的合成路线,并注明必要的反应条件。(无机物任选)_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于温度与反应方向的关系,下列判断不正确的是( )
A.ΔH<0,ΔS>0,所有温度下反应自发进行
B.ΔH>0,ΔS>0,所有温度下反应自发进行
C.ΔH<0,ΔS<0,低温下反应自发进行
D.ΔH>0,ΔS<0,所有温度下反应不能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com