
分析 (1)白色粉末溶解在水中,得到蓝色溶液,说明此溶液中含有铜离子;
(2)向该蓝色溶液中加入AgNO3并加入HNO3,生成白色沉淀且不溶解,说明生成AgCl;
(3)铜离子生成的蓝色沉淀为氢氧化铜,C为氢氧化钾,B为氯化钡,A为硫酸铜,以此解答.
解答 解:(1)白色粉末溶解在水中,得到蓝色溶液,说明此溶液中含有铜离子,则A为铜盐;
(2)在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液,向该蓝色溶液中加入AgNO3并加入HNO3,生成白色沉淀且不溶解,说明生成AgCl,则B为氯化物;
(3)铜离子生成的蓝色沉淀为氢氧化铜,则C为氢氧化钾,可知B为氯化钡,A为硫酸铜,
故答案为:CuSO4;BaCl2;KOH.
点评 本题考查了物质的检验和鉴别,为高频考点,侧重于学生的分析、实验能力的考查,完成本题,需要熟练掌握常见的蓝色沉淀是氢氧化铜,溶液显示蓝色,说明溶液中含有铜离子,本题难度中等.


科目:高中化学 来源: 题型:选择题
| A. | K+ Na+ HSO3- Cl- | B. | Na+ Ba2+[Al(OH)4]- NO3- | ||
| C. | NH4+ K+ Cl- NO3- | D. | Fe2+ Na+ ClO- S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性 F->Cl->Br- | B. | 碱性:Na(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性 HClO4>HBrO4>HIO4 | D. | 稳定性 HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下80gSO2与33.6LCO2含氧原子数目均为3NA | |
| B. | 2molNO与1molO2混合后气体分子数小于2NA | |
| C. | 电解精炼铜时,阳极上粗铜质量减少6.4g,则电路中转化电子数为0.2NA | |
| D. | 1molCnH2n(烯烃)含有的共用电子对数为3nNA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
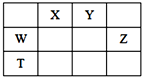 如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 物质WY2、W3X4均有熔点高、硬度大的特性 | |
| D. | T元素的单质不具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
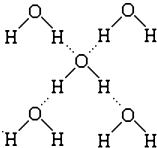 水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.根据下列信息回答问题:
水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.根据下列信息回答问题: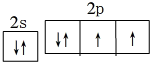
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一定条件下通入氢气发生反应,可除去乙烷中混有的乙烯 | |
| B. | 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴 | |
| C. | 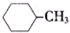 的一氯代物有4种 的一氯代物有4种 | |
| D. | 甲醛溶液与足量的银氨溶液共热的离子反应方程式为:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com