
【题目】下列可以大量共存且形成无色溶液的一组离子应该是( )
A.Ag+、Cu2+、NO3﹣、Na+
B.NO3﹣、Fe3+、Mg2+、SO42﹣
C.Na+、Ca2+、Cl﹣、CO32﹣
D.K+、Ba2+、Cl﹣、NO3﹣
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列属于物理变化的是
A. 麦芽糖和稀硫酸共热
B. 蛋白质溶液中加入饱和NaCl溶液,有沉淀析出
C. 蛋白质溶液中加入浓NaOH溶液
D. 氨基酸中加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其他分散系的本质特征是( )
A.胶体粒子直径在1~100nm之间
B.胶体粒子带电荷
C.胶体粒子能穿过滤纸
D.胶体粒子能够发生布朗运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源可划分为一次能源和二次能源,直接来自于自然界的能源称为一次能源;需依靠其他能源的能量间接制取的能源称为二次能源。下列叙述正确的是( )
A.水煤气是二次能源B.水力是二次能源
C.天然气是二次能源D.电能是一次能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL 0.2mol/L草酸溶液中逐滴加入等浓度的NaOH溶液,溶液中各微粒的物质的量与混合溶液pH的关系如图所示,下列说法正确的是

A. 当V(NaOH溶液)<10mL时,溶液中可能存在:c(Na+)=2c(C2O42-)+c(HC2O4-)
B. 当V(NaOH溶液)=10mL时,溶液中水的电离程度比纯水大
C. 当V(NaOH溶液)=15mL时,溶液中存在: c(Na+)>c(HC2O4-)>c(C2O42-)
D. 当V(NaOH溶液)=20mL时,溶液中存在:c(OH-)=2c(H2C2O4)+c(H+)+c(HC2O4-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,22.4LH2的质量为____________g。
(2)9.8g H2SO4的物质的量为__________mol,约含有___________个氧原子。
(3)VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5L,用水稀释至2VL,则稀释后的溶液中Fe3+的物质的量浓度为_________mol/L。
(4)标准状况下,16 g某气态氧化物RO2的体积为5.6 L。该气体的摩尔质量是________。
(5)b%的硫酸溶液与4b%的硫酸溶液等体积混合后,所得溶液的质量分数______(填 <、>或 = 下同)2.5b%。
(6)在某温度时,一定量的元素A的气态氢化物AH3,在一定体积的密闭容器中完全分解成两种气体单质,此时压强增加了75%,则单质A的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钠、氯化钠和氧化镁等离子晶体的核间距和晶格能(部分)如下表所示

(1)溴化钠晶体比氯化钠晶体晶格能________(填“大”或“小”),主要原因是_____。
(2)氧化镁晶体比氯化钠晶体晶格能大,主要原因是_________________________________。
(3)溴化钠、氯化钠和氧化镁晶体中,硬度最大的是________。工业制取单质镁时,往往电解的是氯化镁而不是氧化镁,主要原因是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随1g![]() 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
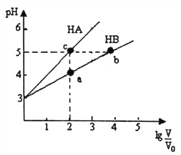
A. 稀释相同倍数时:c(Aˉ)>c(Bˉ-)
B. 水的电离程度:b=c>a
C. 溶液中离子总物质的量:b>c>a
D. 溶液中离子总浓度:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,以乙烯为原料生产部分化工产品的反应如下(部分反应条件已略去):
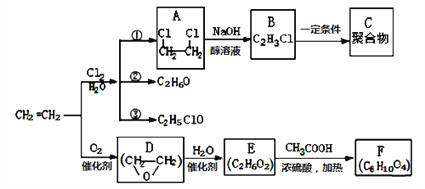
请完成下列问题:
(1)A的名称是___________,C的结构简式为_____________。
(2)E和CH3COOH反应生成F的化学方程式为____________,该反应的类型________。
(3)②和③是副反应,写出C2H5ClO的结构简式_________________________________。
(4)写出D的稳定同分异构体的结构简式____________。检验该同分异构体的实验步骤为_______________________________。
(5)高聚物C也可以用电石(CaC2)为主要原料来合成,写出其合成路线。____________________(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com