
| A£®³ĪĒåŹÆ»ŅĖ®ÖŠµĪ¼ÓĻ”ĮņĖį£ŗCa(OH)2+2H+====Ca2++2H2O |
| B£®ŹµŃéŹŅÓĆ°±Ė®ÖʱøÉŁĮæAl(OH)3£ŗAl3++ 3OH-====Al(OH)3”ż |
| C£®ĻņFeBr2ČÜŅŗÖŠĶØČė¹żĮæĀČĘų£ŗ2Fe2++Cl2====2Fe3++2Cl- |
| D£®ĻņNaOHČÜŅŗÖŠµĪ¼ÓĶ¬ÅØ¶ČµÄÉŁĮæCa(HCO3)2ČÜŅŗ£ŗ |
 +2OH-====CaCO3”ż+
+2OH-====CaCO3”ż+ +2H2O
+2H2O ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Cl2ÓėH2O·“Ó¦£ŗCl2+H2O=2H++Cl-+ClO- |
| B£®Ģ¼ĖįĒāÄĘČÜŅŗÓėĻ”ĮņĖį·“Ó¦£ŗCO32-+2H+=CO2”ü+H2O |
| C£®Al2(SO4)3ČÜŅŗÓė°±Ė®·“Ó¦£ŗAl3+ +3OH-=Al(OH)3”ż |
| D£®NaÓėH2O·“Ó¦£ŗ2Na + 2H2O = 2Na+ + 2OH - +H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| pH | 6.5”«6.8 |
| Ca2+”¢Mg2+×ÜÅØ¶Č | <0.0045mol/L |
| Ļø¾ś×ÜŹż | <100øö/L |
 Ņ»¼¶³Į½µ³Ų
Ņ»¼¶³Į½µ³Ų ¶ž¼¶³Į½µ³Ų
¶ž¼¶³Į½µ³Ų  ¹żĀĖ³Ų”ś×ŌĄ“Ė®
¹żĀĖ³Ų”ś×ŌĄ“Ė®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĀČĘųČÜÓŚĖ®£ŗH2O + C122H+ + ClO- + Cl- |
| B£®½«ĀĮ·ŪĶ¶ČėĒāŃõ»ÆÄĘČÜŅŗÖŠ£ŗ2Al + 2OH-+6H2O2[Al(OH)4]- + 3H2”ü |
| C£®Ģś·ŪÓėĀČ»ÆĢśČÜŅŗ·“Ó¦£ŗFe + Fe3+2Fe2+ |
| D£®Ļ”ĮņĖįÓėĒāŃõ»Æ±µČÜŅŗ»ģŗĻ£ŗSO42- + H+ + Ba2+ + OH-H2O + BaSO4”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ė®µēĄė²śÉśµÄc(H+)£½1”Į10£12mol/LµÄČÜŅŗÖŠ£ŗAlO2£”¢S2£”¢PO43£”¢Na+ |
| B£®¼ÓČė½šŹōĆ¾ÄܲśÉśH2µÄČÜŅŗÖŠ£ŗNa+”¢HCO3£”¢SO42-”¢Al3+ |
| C£®ÄÜŹ¹AlČܽā²śÉśH2µÄČÜŅŗÖŠ£ŗNH4+”¢Na+”¢SiO32£”¢CO32£ |
| D£®ŗ¬ÓŠ“óĮæFe2+µÄČÜŅŗÖŠ£ŗK+”¢Mg2+”¢ClO£”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓĆĻ”ĮņĖį³żČ„ĶĀĢ£ŗ4H£«£«Cu2(OH)2CO3===2Cu2£«£«CO2”ü£«3H2O |
| B£®½«Na2O2¹ĢĢåĶ¶ČėH218OÖŠ£ŗ2H218O£«2Na2O2===4OH££«4Na£«£«18O2”ü |
| C£®ĻņNH4Al£ØSO4£©2ČÜŅŗÖŠµĪČėBa(OH)2ČÜŅŗĒ”ŗĆŹ¹SOĶźČ«³Įµķ£ŗ2Ba2£«£«NH£«Al3£«£«2SO£«4OH£===Al(OH)3”ż£«NH3”¤H2O£«2BaSO4”ż |
| D£®ĻņNa2FeO4ČÜŅŗÖŠ¼ÓČėĻ”ĮņĖį²śÉśŃõĘų£ŗ4FeO£«20 H£«===4Fe3£«£«3O2”ü£«10H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĀĮ·ŪĶ¶Čėµ½NaOHČÜŅŗÖŠ£ŗ2Al+2OH£ØTØT 2AlO2£+H2”ü |
| B£®ĢśĘ¬Ķ¶Čėµ½Ļ”ĮņĖįÖŠ£ŗFe + 2H+ ØTØT Fe2+ + H2”ü |
| C£®Ģ¼ĖįøĘ¼ÓČė¹żĮæŃĪĖįÖŠ£ŗCO32£+ 2H+£½CO2”ü + H2O |
| D£®Ņ»Š”æéÄĘĶ¶Čėµ½Ė®ÖŠ£ŗNa + 2H2O = Na+ + 2OH£+ H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®¹żĮæŅŅĖįÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£ŗ2H+£«CO == CO2”ü£« H2O == CO2”ü£« H2O |
| B£®äåŅŅĶéŌŚNaOHĖ®ČÜŅŗÖŠ¼ÓČČ£ŗ CH3CH2Br + NaOH ”śCH2=CH2”ü+NaBr + H2O |
C£®±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĢ¼£ŗ2C6H5O££«CO2£«H2O 2C6H5OH£«CO 2C6H5OH£«CO |
D£®¼×Č©ČÜŅŗÓė×ćĮæµÄŅų°±ČÜŅŗ¹²ČČ£ŗHCHO+4[Ag(NH3)2]++4OH- CO CO +2NH +2NH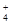 +4Ag”ż+6NH3+2H2O +4Ag”ż+6NH3+2H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com