
����˵������ȷ���ǣ� ��
A����Na2CO3��Һ��ͨ�������CO2����Һ������������
B����8 g SO3 ����92 gˮ�У�������Һ������������Ϊ8 %
C����֪H+(aq) + OH-(aq) = H2O(l)����H = -57.3 kJ/mol����4 g�������ƹ������100 mL
1 mol/L��ϡ�����У��ų���5.73 kJ������
D����100 ml 1 mol/L��Ca(HCO3)2 ��Һ�м����Ũ�ȵ������NaOH��Һ����Һ�ļ��Լ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ƶ��й�����ʵ��ʱ����ʣ����Ӧ�Ż�ԭ�Լ�ƿ | B������25.00 ml ��ʽ�ζ���ȷ��ȡ20.00 ml KMnO4��Һ | C����ʪ��ĵ��۵⻯����ֽ���Լ���NO2��Br2���� | D��ij��Һ�м��������ܲ���ʹ����ʯ��ˮ����ǵ����壬�����Һ��һ������CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ʵ������Ӱ뾶���������Ӱ뾶С | B������ˮ��������Һ����ʹ��ɫ��̪��� | C����ˮ��Ӧʱ��ˮ���������� | D�������ᷴӦ��ֻ����һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ü�ʯ�ҳ�ȥ�����е�ˮ | B���⻯������Ҫ�ĸй���ϣ��廯���������˹����� | C���������ƿ�����DZͧ����������Դ | D����ɫ��Ӧʵ������������ϴ��˿�����պ���մȡ�����ھƾ��������չ۲� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
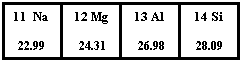 ��ͼΪԪ�����ڱ��������ڵ�һ���֣��ݴ��ж�����˵������ȷ���ǣ�������
��ͼΪԪ�����ڱ��������ڵ�һ���֣��ݴ��ж�����˵������ȷ���ǣ�������| A��SiԪ�ص������ǹ裬��˵����Ϊ14 | B��Mgԭ�ӵĽṹʾ��ͼ��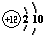 | C��Al�����ԭ��������26.98g | D�����Ƕ����ڽ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��O��Na��SԪ�ص�ԭ�Ӱ뾶�������� | B��KOH��Mg��OH��2��Ba��OH��2�ļ���������ǿ | C��H2SO4��H3PO4��HClO4������������ǿ | D��F2��Cl2��Br2��I2�����������μ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com