
【题目】如图a、b、c、d均为铂电极,供选择的电解质溶液如下表( )
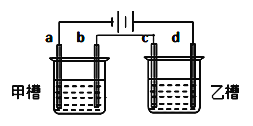
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;
②b、c两极放电离子的物质的量相等。则应选用的电解液是
组 | A | B | C | D |
甲槽 | NaOH | Cu(NO3)2 | KCl | Na2SO4 |
乙槽 | CuSO4 | NaCl | AgNO3 | NaNO3 |
【答案】C
【解析】试题分析:A、甲槽是电解水,氢氧化钠溶液PH增大,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解硫酸铜溶液,溶液PH减小,c电极为阴极,电解反应为:Cu2++2e-=Cu,依据电子守恒可知,b、c两极上反应的离子的物质的量不相等,故A错误;
B、甲槽是电解硝酸铜,溶液PH减小,b电极是阳极,电极反应为:4OH--4e-=2H2O+O2↑;乙槽电解氯化钠,溶液PH增大,c电极是阴极,电极反应为:2H++2e-=H2↑,依据电子守恒可知,b、c两极上反应的离子的物质的量相等,故B错误;
C、甲槽是氯化钾,溶液PH增大,b电极是阳极,电极反应为:2Cl--2e-=Cl2↑;乙槽电解硝酸银溶液,溶液PH减小,c电极为阴极,电解反应为:2Ag++2e-=2Ag,依据电子守恒可知,b、c两极上反应的离子的物质的量相等.故C正确;
D、甲槽是电解水,溶液PH不变;乙槽电解水,溶液PH不变,故D错误。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】利用I2O5可消除CO污染或定量测定CO,反应为:
5CO(g)+I2O5(s)5CO2(g)+I2(s);△H 1
(1)已知:2CO(g)+O2(g)2CO2(g);△H 2
2I2(s)+5O2(g)2I2O5(s);△H 3
则△H 1=(用含△H 2和△H 3的代数式表示).
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图.
请回答:
①c点正反应速率逆反应速率(填“大于”、“等于”或“小于”),a点逆反应速率d点逆反应速率(填“大于”、“等于”或“小于”)
②下列说法正确的是 . (填字母序号)(双选)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应速率的说法中,错误的是( )
A.反应速率可衡量化学反应的快慢
B.决定反应速率的主要因素是反应物的性质
C.增大反应物浓度、提高反应物温度都能增大反应速率
D.因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于现行的元素周期表的说法正确的是( )
A.元素周期表有8个副族
B.元素周期表有18个纵行
C.短周期是指第一、二周期
D.IA族的元素全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:

下列说法不正确的是
A. b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B. 二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
C. 电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6gH2
D. 电解池a极的电极反应式为NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | HCl | NaOH | SO2 | CO2 |
B | NaOH | H2SO4 | NaCl | Na2O | CO2 |
C | KOH | HNO3 | CaCO3 | CaO | CO |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸过程中,SO2的催化氧化是主要反应之一.为了研究外界条件对该反应的影响,将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g)2SO3(g)△H<0,在一定条件下达到平衡,测得c(SO3)=0.040mol/L.
(1)判断该反应达到平衡状态的标志是(填字母)
A.SO2和SO3浓度相等
B.SO2百分含量保持不变
C.容器中气体的压强不变
D.SO3的生成速率与SO2的消耗速率相等
E.容器中混合气体的密度保持不变
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 . (填字母)
A.升高温度
B.降低温度
C.增大压强
D.减小压强
E.加入催化剂 G.移出氧气
(3)计算该条件下反应的平衡常数K= . SO2的平衡转化率为 .
(4)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com