
(13分)
Cl2是一种重要的化工原料。
(1)电解饱和NaCl溶液获得Cl2的化学方程式是_______。
(2)为便于储存,要将氯气液化[ Cl2(g) 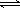 Cl2(l) ],应采取的措施是_______(写出一条即可)。
Cl2(l) ],应采取的措施是_______(写出一条即可)。
(3)液氯储存区贴有的说明卡如下(部分):
危险性 |
|
储运要求 | 远离金属粉末、氨、烃类、醇更物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
包装 | 钢瓶 |
① 用离子方程式表示“泄漏处理”中NaHSO3溶液的作用_______。
② 若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③ 氯气含量检测仪工作原理示意图如下:

Cl2在Pt电极放电的电极反应式是_______。
(4)质量标准要求液氯含水量(以1 g氯气含水的质量计)<0. 4 mg,含水量超标会严重腐蚀钢瓶。液氯含水量的测定装置如下图所示:

(已知:P2O5 + 3H2O = 2H3PO4;Cl2与P2O5不反应。)
① 用离子方程式说明c装置的作用_______。
② 检测液氯的含水量,根据上图,需要测定的数据是_______。
(13分)
(1)2NaCl + 2H2O 电解 2NaOH + H2↑+ Cl2↑
(2)降温 (或加压)
(3)① HSO3- + Cl2 +H2O == SO42- + 2Cl- + 3H+
② 铁与氯气反应生成的氯化铁,对氯与苯的反应有催化作用
③ Cl2 + 2e- + 2Ag+ == 2AgCl
(4)① Cl2 + 2OH- == Cl- + ClO- + H2O
② 分别测定通液氯样品前后a、c 的质量
【解析】
试题分析:(1)电解饱和NaCl溶液生成氢氧化钠、氢气、氯气,化学方程式为2NaCl + 2H2O 电解 2NaOH + H2↑+ Cl2↑
(2)将氯气液化,使Cl2(g) 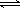 Cl2(l)平衡正向移动,可以加压;气体液化是放热过程,所以还可以降低温度;
Cl2(l)平衡正向移动,可以加压;气体液化是放热过程,所以还可以降低温度;
(3)①NaHSO3溶液与氯气发生氧化还原反应生成硫酸钠和氯化氢,离子方程式为HSO3- + Cl2 +H2O == SO42- + 2Cl- + 3H+;
②钢瓶中含有铁,与氯气反应生成氯化铁,对苯和氯气的反应起催化作用;
③Cl2在Pt电极放电生成氯离子,与银离子结合成氯化银沉淀,从而检测氯气,电极反应式为Cl2 + 2e- + 2Ag+ == 2AgCl
(4)①c装置用于吸收氯气,测定氯气的质量,离子方程式为Cl2 + 2OH- == Cl- + ClO- + H2O
②该装置是检测液氯的含水量,所以需要知道氯气和水的质量,a装置吸收水,c装置吸收氯气,因此需要分别测定通液氯样品前后a、c 的质量。
考点:考查电解饱和食盐水的化学方程式,平衡的移动,离子方程式的书写,装置作用的判断,电化学原理的应用


科目:高中化学 来源:2013-2014北京市西城区下学期高二年级期末考试化学试卷(解析版) 题型:实验题
(12分)
Ⅰ. 实验室制得气体中常含有杂质,影响其性质检验。
下图A为除杂装置,B为性质检验装置,完成下列表格:
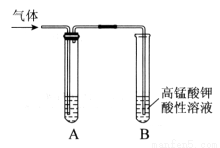
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | ______________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是________________________ | NaOH溶液 |
③ | 乙炔 | 电石与饱和食盐水反应 | _______________ |
Ⅱ. 为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
试管编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是________________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是________________________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_______________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区下学期高一年级期末考试化学试卷(解析版) 题型:选择题
在下图所示的原电池中,正极发生的反应是
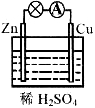
A.2H++2e― H2↑ B.Cu–2e―
H2↑ B.Cu–2e― Cu2+
Cu2+
C.Cu2++2e― Cu D.Zn–2e―
Cu D.Zn–2e― Zn2+
Zn2+
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市海淀区高三第二学期二模理综化学试卷(解析版) 题型:简答题
(14分)
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价, N元素显-3价,用原子结构解释N元素显负价的原因是 ,共用电子对偏向N原子,N元素显负价。
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为 。
(2)含乙酸钠和对氯酚(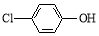 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。
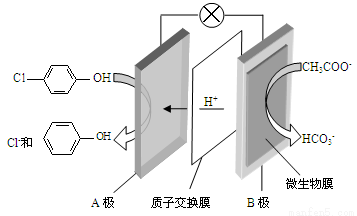
①B是电池的 极(填“正”或“负”);②A极的电极反应式为 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。
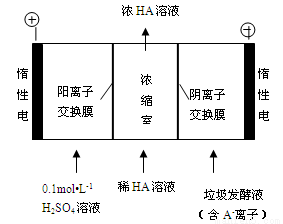
①阳极的电极反应式为 。
②简述浓缩室中得到浓乳酸的原理: 。
③ 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g?L-1乳酸溶液通电一段时间后,浓度上升为145 g?L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为 L。(乳酸的摩尔质量为90 g? mol-1)
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市海淀区高三第二学期二模理综化学试卷(解析版) 题型:选择题
下列有关NH3的实验正确的是
A | B | C | D |
| |
|
|
实验室制NH3 | 证明NH3极易溶于水 | 收集NH3 | 吸收多余NH3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市朝阳区高三二模理综化学试卷(解析版) 题型:选择题
粗制的CuSO4·5H2O晶体中含有Fe2+。提纯时,为了除去Fe2+,常加入少量H2O2, 然后再加入少量碱至溶液pH=4,可以达到除去铁离子而不损失硫酸铜的目的。下列说法不正确的是
A.溶解CuSO4·5H2O晶体时要加入少量稀H2SO4
B.加入H2O2,将Fe2+氧化,2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O
C.由于CuSO4的催化作用,会使部分H2O2分解而损失
D.调溶液pH=4的依据是Cu(OH)2比Fe(OH)3更难溶
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市第二学期期中测试高二化学试卷(解析版) 题型:选择题
为检验某卤代烃中的卤元素,进行如下操作,正确的顺序是
①加热 ②加入AgNO3溶液 ③取少量该卤化物 ④加入足量稀硝酸酸化
⑤加入NaOH溶液 ⑥冷却
A.③①⑤⑥②④ B.③⑤①⑥④② C.③②①⑥④⑤ D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(海南卷解析版) 题型:填空题
(8分)卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多卤代甲烷作为溶剂,其中分子结构为正四面体的是__________。工业上分离这些多卤代甲烷的方法是_______________________。
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式__________(不考虑立体异构)。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下: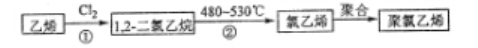
反应①的化学方程式是_____________,反应类型为_______,反应②的反应类型为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com