
(16分) 2SO2(g)+ O2(g) = 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol-1.请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自 身被还原为四价钒氧化物;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式
、 ;
(4)已知单质硫的燃烧热为296 KJ·mol-1,写出硫的燃烧热方程式:
计算由S(s)生成2molSO3(g)的△H KJ·mol-1。
科目:高中化学 来源: 题型:
A.0.4 mol B.0.6 mol C.0.8 mol D.1.2 mol
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期第一次质检化学试卷(解析版) 题型:选择题
恒温恒容条件下,下列叙述正确的是
A.相同的甲、乙两容器中分别加入1 g SO2、1 g O2与2 g SO2、2 g O2,发生反应2SO2(g)+O2(g)  SO3(g)达到平衡,SO2的转化率前者大
SO3(g)达到平衡,SO2的转化率前者大
B.反应2HI(g)  H2(g)+I2(g)达到平衡,增大HI的物质的量,平衡不移动
H2(g)+I2(g)达到平衡,增大HI的物质的量,平衡不移动
C.反应2NO2(g )  N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大
N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大
D.反应2HI(g)  H2(g)+I2(g)达到平衡,增大HI的物质的量,HI的分解率和体积分数均不变
H2(g)+I2(g)达到平衡,增大HI的物质的量,HI的分解率和体积分数均不变
查看答案和解析>>
科目:高中化学 来源:2012届安徽省高二下学期期末联考化学试卷 题型:选择题
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g);ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g);ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
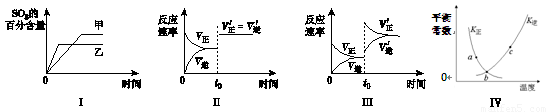
A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态.
查看答案和解析>>
科目:高中化学 来源:09-10学年衡中高二下学期第二次调研考试化学试卷 题型:选择题
下列说法或表示方法正确的是( )
A.反应物的总能量低于生成物的总能量时,该反应一定不能发生
B.化学键和分子间作用力都对物质的性质有一定的影响
 C.已知:2SO2 (g) + O2
(g) 2SO3 (g) ;△H = -98.3
kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
C.已知:2SO2 (g) + O2
(g) 2SO3 (g) ;△H = -98.3
kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0
查看答案和解析>>
科目:高中化学 来源:09-10学年长春外国语学校高一下学期第二次月考理科化学卷 题型:选择题
对于反应2SO2(g)+O2(g) 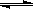 2SO3(g)能增大正反应速率的措施是
2SO3(g)能增大正反应速率的措施是
A.通入大量O2 B.增大容器容积
C.移去部分SO3 D.降低体系温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com