
 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4
软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4分析 (1)根据MnO2+SO2=MnSO4可知,n(SO2)=n(MnO2);
(2)pH=7.1时Mn(OH)2开始沉淀.室温下,除去MnSO4溶液中的Fe3+、Al3+,结合Al(OH)3完全变成沉淀时的pH、Fe(OH)3完全变成沉淀时的pH分析;
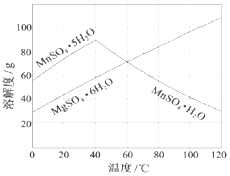
(3)从MnSO4和MgSO4混合溶液中结晶MnSO4•H2O晶体,根据图上信息,高于60℃以后MnSO4•H2O的溶解度减小,而MgSO4•6H2O的溶解度增大,因此控制结晶温度范围是高于60℃;
(4)根据氧化还原反应中得失电子守恒:n(Mn3+)×1=n(Fe2+)×1=0.02L×0.0500mol=1.00×10-3mol,根据Mn元素守恒,m(MnSO4•H2O)=1.00×10-3mol×169g/mol=0.169g,以此计算纯度.
解答 解:(1)根据MnO2+SO2=MnSO4可知,n(SO2)=n(MnO2)=$\frac{17.4g}{87g/mol}$=0.2mol,其体积为0.2mol×22.4L/mol=4.48L,
故答案为:4.48;
(2)pH=7.1时Mn(OH)2开始沉淀.室温下,除去MnSO4溶液中的Fe3+、Al3+,氢氧化铝完全变成沉淀时的pH:Ksp[Al(OH)3]=1×10-33=c(Al3+)×c3(OH-),c(Al3+)=1×10-6mol•L-1,解得:c(OH-)=1×10-9mol•L-1,c(H+)=1×10-5mol•L-1pH=5,同理Fe(OH)3完全变成沉淀时,pH约为3.5,故pH范围是:5.0<pH<7.1,
故答案为:5.0<pH<7.1;
(3)从MnSO4和MgSO4混合溶液中结晶MnSO4•H2O晶体,根据图上信息,高于60℃以后MnSO4•H2O的溶解度减小,而MgSO4•6H2O的溶解度增大,因此控制结晶温度范围是高于60℃这样可以得到纯净的MnSO4•H2O,
故答案为:高于60℃;
(4)根据氧化还原反应中得失电子守恒:n(Mn3+)×1=n(Fe2+)×1=0.02L×0.0500mol=1.00×10-3mol,根据Mn元素守恒,m(MnSO4•H2O)=1.00×10-3mol×169g/mol=0.169g,纯度为$\frac{0.169g}{0.1710g}$×100%=98.8%,
答:根据氧化还原反应中得失电子守恒:n(Mn3+)×1=n(Fe2+)×1=0.02L×0.0500mol=1.00×10-3mol,根据Mn元素守恒,m(MnSO4•H2O)=1.00×10-3mol×169g/mol=0.169g,纯度为$\frac{0.169g}{0.1710g}$×100%=98.8%.
点评 本题考查较综合,涉及氧化还原反应计算、溶度积计算及混合物分离、图象分析等,本题为2015年江苏高考题18题,综合性较强,侧重分析、计算能力的综合考查,题目难度中等.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:选择题
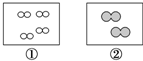 如图所示,①和②为两个体积相同的固定容器,图中“○”和“●”分别表示氢原子和氧原子,则下列说法正确的是( )
如图所示,①和②为两个体积相同的固定容器,图中“○”和“●”分别表示氢原子和氧原子,则下列说法正确的是( )| A. | 若①中的H2为1 mol,则②中所含原子总数为3.01×1023个 | |
| B. | ①和②中气体的质量之比为1:8 | |
| C. | H2、O2均能发生化合反应,但不能发生置换反应 | |
| D. | 两容器的温度和压强均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
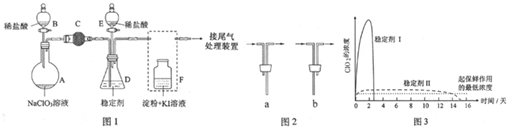
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用10ml量筒量取7.13ml稀盐酸 | |
| B. | 用托盘天平称量25.20g NaCl | |
| C. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| D. | 中和滴定时用去某浓度的碱溶液21.70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度相同、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 压强相等、温度相等的CO和C2H4 | D. | 压强相同、体积相同的N2和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由2H和18O所组成的水11g,其中所含的中子数为5NA | |
| B. | 3NA个NO2分子跟水分子充分作用,转移(偏移)的电子数为2NA | |
| C. | 标准状况下,11.2 L的氧气和氮气的混合物含有的分子数约为NA | |
| D. | 62g白磷晶体中,含2NA个P-P键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmolC2H8N2中含有lmolN2 | |
| B. | 偏二甲肼的摩尔质量为60g | |
| C. | 偏二甲肼是比液氢更环保的燃料 | |
| D. | 偏二甲肼燃烧时能放出大量的热和气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液一定呈酸性 | B. | 该溶液中的c(H+)可能等于10-3 | ||
| C. | 该溶液的pH可能为2,可能为12 | D. | 该溶液有可能呈中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com