
�п��淴ӦFe��s��+CO2��g�� FeO��s�� + CO��g������֪���¶�938Kʱ��ƽ�ⳣ��K=1.5����1173Kʱ��K=2.2 ��
FeO��s�� + CO��g������֪���¶�938Kʱ��ƽ�ⳣ��K=1.5����1173Kʱ��K=2.2 ��
��1��1mol���ۺ�1molCO2��2L�ܱ������з�Ӧ���жϸ÷�Ӧ�ﵽƽ��״̬�������� ������ţ���
A��������ѹǿ���ٸı�
B��c��CO�����ٸı�
C������1mol��FeO
D��c��CO2��=c��CO��
E��v����CO2��=v�棨C O��
O��
��2���÷�Ӧ������Ӧ��_________��ѡ����ȡ��������ȡ�����Ӧ��
��3������ʼʱ��Fe��CO2��������̶����ܱ������У�CO2����ʼŨ��Ϊ2.4 mol/L��ij�¶�ʱ�ﵽƽ�⣬��ʱ������CO��Ũ��Ϊ1.0 mol/L������¶���������Ӧ��ƽ�ⳣ��K= ��������λ��Ч���֣���
��4��һ�������£��÷�Ӧ������̶����ܱ������н���һ��ʱ���ﵽƽ��״̬��ʹ��ƽ��״̬�����ƶ��Ĵ�ʩ�У�д�������� �� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ȤС��̽��SO2���廹ԭFe3��������ʹ�õ�ҩƷ��װ������ͼ��ʾ������˵������������ �� ��
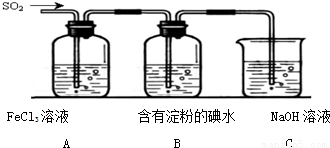
A���ܱ���I���Ļ�ԭ������SO2��������B����ɫ��Һ��ɫ
B��װ��C������������SO2β������ֹ��Ⱦ����
C��Ϊ����֤A�з�����������ԭ��Ӧ��������ϡ�����ữ��BaCl2��Һ��������ɫ����
D��Ϊ����֤A�з�����������ԭ��Ӧ������KMnO4��Һ���Ϻ�ɫ��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��������У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��Դ��������������ͷ�չ����Ҫ���ʻ�����������Դ�ĺ������ú�����Դ�Ŀ����ǵ�������������ٵ��Ͼ����⡣�ش��������⣺
��1���ҹ���������������úΪ��Ҫȼ�ϵĹ��ң����й���ú��ȼ�ϵ��۵���ȷ����_______
A��ú����Ҫ�Ļ���ԭ�ϣ���ú��ȼ�ϼ�ȼ�յ�̫��ϧ��Ӧ���ۺ�����
B��ú�Ƿ��ȺܸߵĹ���ȼ�ϣ��ҹ�ú̿��Դ��Լ��У����ɳɱ��ͣ���ú��ȼ�Ϻ���
C��úȼ��ʱ������������������̳����Ի�����Ⱦ����
D��ͨ���ྻú��������ú��������Һ���Լ����� ������������ȼú��Ⱦ���������úȼ�յ���������
������������ȼú��Ⱦ���������úȼ�յ���������
��2���ڿ�����ѧ�ҽ�ͭ��������ۻ��Ƴɶ��������������̫�ջ����ʹ�õ�ú��ȼ��������������������������_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��������У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�й�X��Y��Z��W���ֽ�����������ʵ�飺
1 | ��X��Y�õ������ӣ�����������Һ�У�Y����ʴ |
2 | ��Ƭ״��X��W�ֱ�Ͷ���Ũ�������ж������������W��X��Ӧ���� |
3 | �ö��Ե缫�������ʵ���Ũ�ȵ�Y��Z�������λ����Һ���������������� |
����������ʵ�������жϻ��Ʋ�������
A��Z����������������ǿ
B��W�Ļ�ԭ��ǿ��Y�Ļ�ԭ��
C��Z����CuSO4��Һ��һ����Cu����
D����X��Z��ϡ����ɹ���ԭ��أ���X������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��������У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��һ��������ij���ȷ�Ӧ���Է����У�˵���÷�Ӧ��������ķ�Ӧ
B.����Ӧ��Ũ�ȿɼӿ췴Ӧ���ʣ���˿���Ũ����������Ӧ������ ��H2������
��H2������
C�������ɼӿ췴Ӧ���ʲ�Ӱ��ƽ����ƶ�
D������Ӧ���������ɴ�ʹƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ����������ѧ�Ծ��������棩 ���ͣ�ѡ����
���жԻ�ѧƽ���ƶ��ķ����У�����ȷ���ǣ� ��
���Ѵ�ƽ��ķ�ӦC��s��+H2O��g�� CO��g��+H2��g�������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
CO��g��+H2��g�������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
���Ѵ�ƽ��ķ�ӦN2��g��+3H2��g�� 2NH3��g��������N2��Ũ��ʱ��ƽ��һ��������Ӧ�����ƶ�
2NH3��g��������N2��Ũ��ʱ��ƽ��һ��������Ӧ�����ƶ�
���Ѵ�ƽ��ķ�ӦA��g����B��g�� C��g����D��g���������¶ȣ�A�ķ�Ӧ����������ƽ��һ�������ƶ�
C��g����D��g���������¶ȣ�A�ķ�Ӧ����������ƽ��һ�������ƶ�
���Ѵ�ƽ��ķ�ӦH2��g�� + I2��g��  2HI��g������ѹ�����³��뺤����ƽ�ⲻ�ƶ�
2HI��g������ѹ�����³��뺤����ƽ�ⲻ�ƶ�
A���٢� B���ۢ� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ����������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��C��s����O2��g��=CO2��g�� ��H1=��395kJ/mol��
CO��g����1/2O2��g��=CO2��g�� ��H2=��283kJ/mol��
��ӦC��s����1/2O2��g��=CO��g���ķ�Ӧ�ȡ�H3���� ? ?
A�� ��112 kJ/mol B����395 kJ/mol C��+ 112 kJ/mol D����283 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ�������ɽ�ظ��������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ʾ��ȷ����
A������ʯ��ˮ��ͨ�����������̼��OH����CO2=HCO3��
B��ͭƬ�����Ȼ�����Һ��Ӧ��Fe3+��Cu=Cu2+��Fe2+
C��Ư����Һ��ͨ������SO2��Ca2++2ClO��+SO2+H2O=CaSO3��+2HClO
D��Fe3O4��ϡHNO3��Ӧ��Fe3O4��8H+=Fe2+��2Fe3+��4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ������У�߶���ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��Ȼ�ѧ����ʽ��������ȷ���ǣ� ��
A��2H2��g����O2��g��=2H2O��g������H=��483.6 kJ/mol����������ȼ����Ϊ241.8 kJ
B����֪C��ʯī��s��= C�����ʯ��s�� ��H��0������ʯ��ʯī�ȶ�
C����20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ��NaOH��aq����HCl��aq��=NaCl��aq����H2O��l������H=��57.4 kJ/mol
D����֪2C��s����2O2��g��=2CO2��g������H1 ��2C��s����O2��g��=2CO��g�� ��H2�����H1����H2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com