
【题目】NA表示阿伏伽德罗常数的值,下列叙述不正确的是
A. 60g SiO2晶体含4NA个σ键
B. 1mol[Cu(NH3)4]2+中含4NA配位键
C. 在24g石墨中,含C-C共价键数目为6NA
D. CO和N2是等电子体,标况下22.4L的CO气体与1molN2所含的电子数相等
【答案】C
【解析】A.60gSiO2晶体的物质的量为1mol,含有4molSi—O键,即含4NA个σ键,故A正确;B.[Cu(NH3)4]2+中中心离子Cu2+与配体NH3间存在配位键,则1mol[Cu(NH3)4]2+中含4NA配位键,故B正确;C.2.4g石墨含有的碳原子的物质的量为0.2mol,每个碳原子与其它碳原子形成了3个碳碳键,每个碳原子形成的共价键为: ![]() ×3=1.5个,所以0.2molC形成了0.3mol共价键,含C-C共价键数目为0.3NA,故C错误;D.CO和N2是等电子体,均含有14个电子的分子,则标况下22.4L的CO气体与1molN2所含的电子数相等,故D正确;答案为C。
×3=1.5个,所以0.2molC形成了0.3mol共价键,含C-C共价键数目为0.3NA,故C错误;D.CO和N2是等电子体,均含有14个电子的分子,则标况下22.4L的CO气体与1molN2所含的电子数相等,故D正确;答案为C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是
A. Na+ 、Mg2+ 、Cl- 、SO42- B. Na+ 、Ca2+ 、CO32- 、NO3-
C. Na+ 、H+ 、Cl- 、CO32- D. K+ 、Al3+ 、SO42- 、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素[CO(NH3)2]
已知:①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-159.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为______________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40molCH4和1.0molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如右图所示:
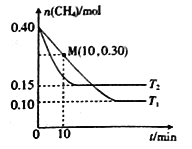
①根据右图判断该反应的△H________0(填“>”、“<”或“=”),理由是______________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO2)=__________,反应的平衡常数K=___(保留三位小数)
③该反应达到平衡后,为在提高反应速率同时提高NO2的转化率,可采取的措施有______(填标号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH________(填“增大”、“减小”或“不变”),负极的电极反应式为___________________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为________;常温下,将amol·L-1 的HN3与bmol·L-1 的Ba(OH) 2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈_______(填“酸”、“碱”或“中”)性,溶液中c(HN3)=_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3 C.X2YZ2 D.XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2是一种橙黄色的液体,遇水剧烈反应,并产生能使品红褪色的气体。下列说法错误的是

A. S2Cl2的分子中的两个S原子均是sp3杂化
B. S2Br2与S2Cl2结构相似,熔沸点:S2Br2 > S2Cl2
C. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O = SO2↑+3S↓+4HCl
D. S2Cl2分子中的S为+1价,是含有极性键和非极性键的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是

A. H2R是二元弱酸,其Ka1=1×10-2
B. NaHR在溶液中水解程度小于电离程度
C. pH<7.2的溶液中一定存在:c( Na+)>c( HR-) > c(R2- )>c(H+)>c(OH-)
D. 含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应生成1molH2O时会放出57.3kJ的热量
B. 由C(石墨,s)——C(金刚石,s)△H=+1.9 kJmol-1可知,石墨比金刚石更稳定
C. 在500℃、MPa下,将0.5 mol N2和l.5 mol H2置于密闭容器中充分反应生成NH3,放热19.3kJ,则其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6 kJmol-1
2NH3(g) △H=-38.6 kJmol-1
D. 甲烷的燃烧热(△H)为-890.3 kJmol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) △H=-890.3 kJmol-1
CO2(g)+2H2O(g) △H=-890.3 kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池中通入CH4电极的电极反应为___________________________________。
(2)乙池中A(石墨)电极的名称为________(填“正极”、“负极”或“阴极”、“阳极”), 乙池中总反应式为____________________________________ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为______mL(标准状况),丙池中______(填“C”或“D”)极析出_______g铜。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com