
| A、金属钠保存在煤油中 |
| B、存放FeSO4溶液时加入少量铁粉 |
| C、NaOH溶液保存在带橡胶塞的玻璃试剂瓶中 |
| D、FeCl3溶液保存在广口瓶中 |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
| A、在盐酸溶液中,AgCl的溶解度会减小 |
| B、向存在AgCl沉淀的少量溶液中加入NaI固体,会生成黄色沉淀 |
| C、向AgNO3溶液中加入足量盐酸,反应后的溶液中没有Ag+ |
| D、达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
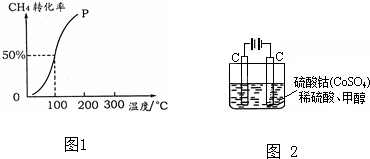
| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 物 质 | 杂 质 | 所 用 试 剂 |
| A | N2 | O2 | 灼热的铜网 |
| B | CO2 | H2O | 浓硫酸 |
| C | CaO | CaCO3 | 适量的稀盐酸 |
| D | NaCl溶液 | Na2CO3 | 适量的稀盐酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
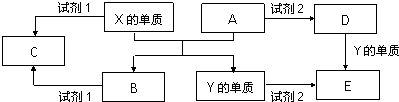
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3++3OH-═Fe(OH)3↓ |
| B、Zn+Cu2+═Zn2++Cu |
| C、2H2O2═2H2O+O2↑ |
| D、2H2S+SO2═3S↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时氨气为2.5mol | ||
| B、平衡时HI的分解率为20% | ||
| C、若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol | ||
D、其他条件不变把容器的体积缩小到
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com