
【题目】实验室欲使1.6 g Fe2O3完全被还原,事先应准备的CO气体的标准状况下的体积为( )
A. 672 mLB. 336 mLC. 大于672 mLD. 小于336 mL
科目:高中化学 来源: 题型:
【题目】将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(假设还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。

(1)生成的NO在标况下的体积为___________L。
(2)Cu的物质的量为_________mol。
(3)稀硝酸的浓度为___________mol/L。
(4)a的值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图。
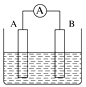
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是__(填字母)。
A 铝片、铜片 B 铜片、铝片
C 铝片、铝片 D 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:___;该电池在工作时,A电极的质量将_(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:_________;该电池在工作一段时间后,溶液的碱性将___(填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:________;若该电池反应消耗了6.4克CH4,则转移电子的数目为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将35g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2L(标准状况),其质量为19.6g,则剩余锌粉的质量为
A. 1.0g B. 2.0g C. 2.5g D. 3.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列化合物:①NaCl②NaOH③HCl④FeCl3⑤CH3COONa⑥CH3COOH⑦NH3H2O⑧H2O
请回答下列问题:
(1)FeCl3溶液显__________性,用离子方程式表示______________________;
CH3COOH溶液显________性,用离子方程式表示__________________________;
(2)常温下,pH=10的CH3COONa溶液中,水电离出来的c(OH-)=_________________;
在pH=3HCl的溶液中,水电离出来的c(H+)=___________________;
(3)已知水存在如下平衡:H2O+H2O![]() H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择方法是____________。
H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择方法是____________。
A.向水中加入NaHSO4固体
B.向水中加入(NH4)2SO4固体
C.加热至100℃[其中c(H+)=1×10-6molL-1]
D、向水中加Na2CO3固体
(4)若等浓度、等体积的②NaOH和⑦NH3H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH相等,则m___________n(填“<”、“>”或“=”)。
(5)25℃,pH=a的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va_____Vb(填“>”、“<”、“=”、“无法确定”)
(6)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为:______________________________________________(填序号)。
(7)常温下pH=13的NaOH溶液与pH=2的盐酸溶液混合,所得混合液的pH=11,则NaOH与盐酸的体积比为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合,只要物质的量之和不变,完全燃烧时所消耗的氧气量和生成水的物质的量也分别不变。则下列有关判断正确的是 ( )
A. X、Y分子式中氢原子数一定要相同,碳原子数必定相同
B. 若X为CH4,则相对分子质量最小的Y是甲醇
C. 若X为CH4,则相对分子质量最小的Y是乙二醇
D. X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得沉淀20g 滤液质量比原石灰水减少5.8g,该有机物不可能是( )
A. 乙烷 B. 乙醇 C. 乙烯 D. 乙二醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种主族元素的离子![]() 、
、![]() 、
、![]() 、
、![]() (a、b、c、d 为元素的原子序数),它们具有相同的电子层结构,若 m>n,对下列叙述的判断正确的是( )
(a、b、c、d 为元素的原子序数),它们具有相同的电子层结构,若 m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数 a>b>c>d ③元素非金属性 Z>R ④最高价氧化物对应水化物碱性 X>Y
A.③B.①②③④C.①②③D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是 ( )
A. 用溴水可鉴别苯、乙醇、苯乙烯![]()
B. 加浓溴水,然后过滤可除去苯中少量乙烯
C. 苯、溴水、铁粉混合制成溴苯
D. 可用分液漏斗分离硝基苯和苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com