
| A. | B也可在O2作用下直接转化为D | |
| B. | 当X是强酸时,A可能是Na2S,F是H2SO4 | |
| C. | 当X是强碱时,过量的B与Cl2发生的反应为:3Cl2+2NH3═N2+6HCl | |
| D. | 无论X是强酸还是强碱,在一定条件下,B和D都能相互反应生成C单质 |
分析 根据图中的转化关系可知,A一定是弱酸的铵盐,因此当X是强碱时,B是氨气,则C是氮气,D是NO,E是NO2,F是硝酸;如果X是强酸,则B应该是H2S,C是S,D是SO2,E是三氧化硫,F是硫酸,这说明A是硫化铵,据此答题.
解答 解:根据图中的转化关系可知,A一定是弱酸的铵盐,因此当X是强碱时,B是氨气,则C是氮气,D是NO,E是NO2,F是硝酸;如果X是强酸,则B应该是H2S,C是S,D是SO2,E是三氧化硫,F是硫酸,这说明A是硫化铵,
A、B可能是氨气,也可能是硫化氢,氨气与氧气生成一氧化氮,硫化氢与氧气反应生成二氧化硫,D是NO或SO2,故A正确;
B、当X是强酸时,A可能是Na2S,B是H2S,C是S,D是SO2,E是三氧化硫,F是H2SO4,故B正确;
C、当当X是强碱时,B是氨气,过量的B与Cl2发生的反应为:3Cl2+8NH3═N2+6NH4Cl,故C错误;
D、无论X是强酸还是强碱,根据上面的分析可知,B是氨气、D是NO或者B是H2S、D是SO2,在一定条件下,B和D反应生成氮气或硫单质,故D正确,
故选C.
点评 本题考查考查S和N元素及其化合物转化的有关判断,是中等难度的试题,也是高考中的常见题型.试题注重基础和能力的双向考查,该题的突破点是有关的反应条件以及能和强碱反应生成气体.本题有利于培养学生的逻辑思维能力,提高学生分析问题、解决问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | b<a<0 | B. | b>d>0 | C. | 2a=d>0 | D. | 2b=c<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
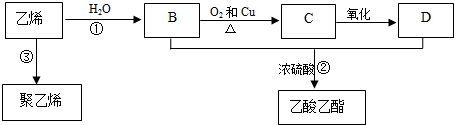
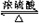 CH3COOC2H5+H2O.
CH3COOC2H5+H2O. +CaCl2+H2O
+CaCl2+H2O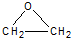
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (用电子式表示).
(用电子式表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑥ | C. | ⑤⑦ | D. | ⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
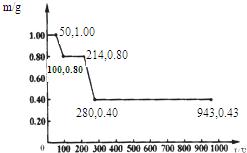 (1)用甲烷制氢是一种廉价的制氢方法.有关的热化学方程式如下:
(1)用甲烷制氢是一种廉价的制氢方法.有关的热化学方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
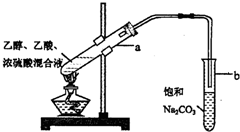
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3的摩尔质量为71g | |
| B. | 还原剂和氧化剂的物质的量之比是2:1 | |
| C. | 若生成0.2mol HNO3,则转移0.2mol电子 | |
| D. | NF3在潮湿的空气中泄漏可观察到红棕色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com