
【题目】CO2催化加氢制甲醇,是极具前景的温室气体资源化研究领域。在某CO催化加氢制甲醇的反应体系中,发生的主要反应有:
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g) ![]() CH3OH(g) △H3
CH3OH(g) △H3
(1)△H3________ kJ·mol-1
(2)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
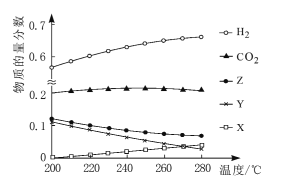
①体系中CO2的物质的量分数受温度的影响不大,原因是____。
②250℃时,反应ii的平衡常数____1(填“>”“<”或“=”)。
③下列措施中,无法提高甲醇产率的是____(填标号)。
A 加入适量CO B 增大压强 C 循环利用原料气 D 升高温度
④如图中X、Y分别代表____(填化学式)。
(3)反应i可能的反应历程如下图所示。
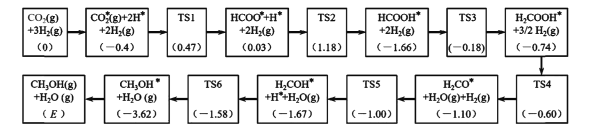
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中,TS表示过渡态、*表示吸附在催化剂上的微粒。
①反应历程中,生成甲醇的决速步骤的反应方程式为____。
②相对总能量E=____(计算结果保留2位小数)。(已知:leV=1.6×10-22kJ)
(4)用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,往电解池的____极通入氢气,阴极上的电极反应为____。
【答案】-90.6 温度改变时,反应i和反应ii平衡移动方向相反 < D CO、CH3OH HCOOH*+2H2(g)=H2COOH*+3/2H2 -0.51 阳 CO2+6e-+6H+=CH3OH+H2O
【解析】
(1)已知:
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g) ![]() CH3OH(g) △H3
CH3OH(g) △H3
根据盖斯定律可知反应i-ii可得反应iii,所以△H3=△H1-△H2=-49.4kJ/mol-41.2kJ/mol=-90.6kJ/mol;
(2) △H1<0,△H3<0,即生成甲醇的反应均为放热反应,所以温度升高平衡时甲醇的物质的量分数应减小,△H2>0,生成CO的反应为吸热反应,所以随温度升高CO平衡时的物质的量分数会变大,二者共同作用导致水蒸气减小幅度小于甲醇,所以Z代表H2O,Y代表CH3OH,X代表CO。
①依据主要反应的化学方程式可知,反应i消耗CO2,反应ii逆向产生CO2,最终体系内CO2的物质的量分数与上述两个反应进行的程度相关。由于△H1<0而△H2>0,根据勒夏特列原理,温度改变时,反应i和反应ii平衡移动方向相反,且平衡移动程度相近,导致体系内CO2的物质的量分数受温度的影响不大;
②反应ii平衡常数K=![]() ,该反应前后气体体积计量数之和不变,所以可以用物质的量分数来代表浓度估算K值,据图可知250℃时,CO2与H2的物质的量分数大于CO和H2O的物质的量分数,所以K<1;
,该反应前后气体体积计量数之和不变,所以可以用物质的量分数来代表浓度估算K值,据图可知250℃时,CO2与H2的物质的量分数大于CO和H2O的物质的量分数,所以K<1;
③A. 加入适量CO,促使反应iii平衡正向移动,产生更多的CH3OH,而反应ii平衡逆向移动,又可减少CO2转化为CO,使更多的CO2通过反应i转化为CH3OH,故CH3OH产率提高,A项正确;
B. 增大压强,有利于反应i和iii的平衡正向移动,而对反应ii无影响,B项正确;
C. 循环利用原料气能提高CO2的转化率,使CH3OH的产率提高,C项正确;
D. 由图可知,升温,CH3OH的物质的量分数下降,产率降低,D项错误;
综上所述选D;
④根据分析可知X代表CO,Y代表CH3OH;
(3)①生成CH3OH的决速步骤,指反应历程中反应速率最慢的反应。速率快慢则由反应的活化能决定,活化能越大,反应速率越慢。仔细观察并估算表中数据,找到活化能(过渡态与起始态能量差)最大的反应步骤为:HCOOH*+2H2(g)=H2COOH*+3/2H2,Ea=-0.18-(-1.66)= 1.48 eV;
②反应i的△H1= -49.4kJ/mol,指的是1mol CH3OH(g)和1molH2O(g)的总能量与1 mol CO2(g)和3mol H2(g
E=![]() =
=![]() =-0.51eV;
=-0.51eV;
(4)因为电解过程CO2被还原为CH3OH,H2应发生氧化反应,故氢气通入阳极附近溶液中;而阴极上CO2转化为CH3OH,碳元素从+4价降为-2价,电解质溶液为硫酸,所以电极方程式为:CO2+6e-+6H+=CH3OH+H2O。


科目:高中化学 来源: 题型:
【题目】利用反应 NO2+NH3→N2+H2O(未配平)制作下面装置图所示的电池,用以消除氮氧化物的污染。下列有关该电池说法一定正确的是 ( )

A.电极乙为电池负极
B.离子交换膜为质子交换膜
C.负极反应式为 2NH3-6e-+6OH-=N2↑+6H2O
D.28.0L(标准状况)NO2 完全被处理,转移 4mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是分离混合物时常用的仪器,可以进行的混合物分离操作分别是()
![]()
A.蒸馏、过滤、萃取、蒸发B.蒸馏、蒸发、萃取、过滤
C.萃取、过滤、蒸馏、蒸发D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 能自发进行的反应一定能迅速发生
B. 非自发进行的反应一定不可能发生
C. 能自发进行的反应实际可能没有发生
D. 常温下发生反应2H2O![]() 2H2↑ + O2↑,说明常温下水的分解反应是自发反应
2H2↑ + O2↑,说明常温下水的分解反应是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X 、Y、Z 的原子序数依次增大,W、X 同主族,Y原子的最外层电子数等于X原子的电子总数,Z原子的电子总数等于W、X、Y 三种原子的电子数之和,Z的最高价氧化物对应水化物的化学式为HnZO2n+2 。W、X、Y 三种元素形成的一种化合物的结构如图所示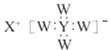 。下列说法错误的是
。下列说法错误的是
A.X常用来制造电池
B.Y、Z形成的化合物常用于制取单质Y
C.W的简单离子半径可能大于X的简单离子半径
D.Z的单质的水溶液需保存在棕色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,醋酸溶液中存在下述关系:Ka=c(H+)c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中Ka的数值是该温度下醋酸的电离平衡常数。有关Ka的下列说法正确的是( )
A. 当向该溶液中加入一定量的硫酸时,Ka的值增大
B. 升高温度,Ka的值增大
C. 向醋酸溶液中加水,Ka的值增大
D. 向醋酸溶液中加氢氧化钠溶液,Ka的值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组制备消毒液(主要成分是NaClO),设计了下列装置。
已知:Cl2和NaOH溶液能发生下列反应
在加热时:![]()
在低温时:![]()
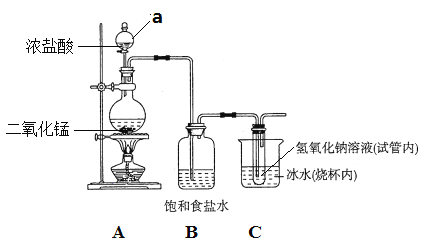
试回答下列问题:
⑴仪器a的名称是_____________。
⑵连接好装置,装药品之前,必须进行的一项操作是_________________。
⑶A装置内发生反应的化学方程式为_______________________________。
⑷B的作用是___________;冰水的作用是__________________________。
⑸该装置的不足之处有___________________________________________。
⑹一定温度下,向NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
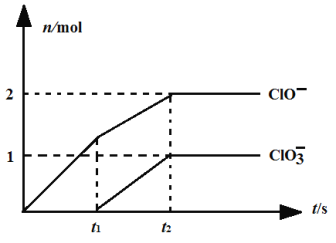
该过程中t2时刻参加反应的Cl2物质的量为_________mol;若另一过程产生的n(Cl-)为5.5mol,n(ClO3-)为1mol,则参加反应的NaOH物质的量为___________________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大型客机燃油用四乙基铅[Pb(CH2CH3)4])做抗震添加剂,但皮肤长期接触四乙基铅对身体健康有害,可用硫基乙胺(HSCH2CH2NH2)和KMnO4清除四乙基铅。
(1)碳原子核外电子的空间运动状态有______种,基态锰原子的外围电子排布式为___,该原子能量最高的电子的电子云轮廓图形状为________。
(2)N、C和Mn电负性由大到小的顺序为____________。
(3)HSCH2CH2NH2中C的杂化方式为_____,其中NH2-空间构型为____;N和P的价电子相同,但磷酸的组成为H3PO4,而硝酸的组成不是H3NO4,其原因是_______。
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于_____晶体。已知Pb(CH2CH3)4晶体的堆积方式如下。
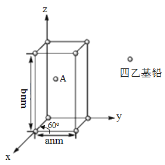
Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是___,A分子的坐标参数为_____;设阿伏加德罗常数为NA/mol,Pb(CH2CH3)4]的摩尔质量为Mg/mol,则Pb(CH2CH3)4]晶体的密度是_____g/cm3 (列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
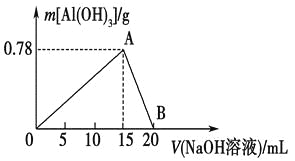
(1)图中A点表示的意义是_________________________。
(2)图中B点表示的意义是_________________________。
(3)上述两步反应用总的离子方程式可表示为:____________________________。
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com