
·ÖĪö £Ø1£©Fe2+ŗĶFe3+µÄ×Ŗ»Æ£¬FeŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ĢåĻÖ»¹ŌŠŌ£»FeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ĢåĻÖŃõ»ÆŠŌ£»
£Ø2£©Ī¬ÉśĖŲCæÉŅŌŹ¹Ź³ĪļÖŠµÄFe3+»¹Ō³ÉFe2+£¬FeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņĪ¬ÉśĖŲC֊ijŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ»
£Ø3£©FeÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĒāĘų£»
£Ø4£©·“Ó¦ŗóCO2×Ŗ±ä³ÉÓŠ»śĪļ¼×Č©£¬CŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņFeŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ®
½ā“š ½ā£ŗ£Ø1£©Fe2+ŗĶFe3+µÄ×Ŗ»Æ£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬ĢśĄė×Ó¾ßÓŠŃõ»ÆŠŌ£¬¹Ź“š°øĪŖ£ŗ»¹Ō£»Ńõ»Æ£»
£Ø2£©Ī¬ÉśĖŲCæÉŅŌŹ¹Ź³ĪļÖŠµÄFe3+»¹Ō³ÉFe2+£¬FeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņĪ¬ÉśĖŲC֊ijŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ŌņĪ¬ÉśĖŲC¾ßÓŠ»¹ŌŠŌ£¬×÷»¹Ō¼Į£¬¹Ź“š°øĪŖ£ŗ»¹Ō£»»¹Ō£»
£Ø3£©FeÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĒāĘų£¬·¢ÉśµÄ·“Ó¦ĪŖFe+2HCl=FeCl2+H2”ü£¬Ąė×Ó·“Ó¦ĪŖFe+2H+=Fe2++H2”ü£¬¹Ź“š°øĪŖ£ŗFe+2HCl=FeCl2+H2”ü£»Fe+2H+=Fe2++H2”ü£»
£Ø4£©·“Ó¦ŗóCO2×Ŗ±ä³ÉÓŠ»śĪļ¼×Č©£¬CŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņFeŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ®£Ø1£©£Ø2£©£Ø3£©£Ø1·Ö£©
£Ø4£©·“Ó¦ŗóCO2×Ŗ±ä³ÉÓŠ»śĪļ¼×Č©£¬CŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņFeŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬Ōņ¶žŃõ»ÆĢ¼×÷Ńõ»Æ¼Į£¬·¢ÉśµÄŃõ»Æ»¹Ō·“Ó¦µÄĄė×Ó·“Ó¦ĪŖCO2+4Fe2++5H2O=CH2O+2Fe2O3+8H+£¬
¹Ź“š°øĪŖ£ŗŃõ»Æ£»CO2+4Fe2++5H2O=CH2O+2Fe2O3+8H+£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĻ°ĢāÖŠµÄŠÅĻ¢¼°·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėĒØŅĘÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ·ÖÉ¢ĻµµÄ·ÖĄą | |
| B£® |  “×ĖįĻ”ŹĶ | |
| C£® | 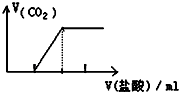 ĻņNa2CO3ČÜŅŗÖŠÖšµĪµĪČėŃĪĖį | |
| D£® | 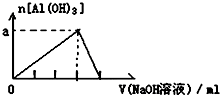 ĻņAlCl3ČÜŅŗÖŠµĪ¼Ó¹żĮæµÄNaOHČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ü | B£® | ¢Ł¢Ū¢Ü | C£® | ¢Ū | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
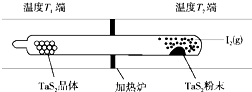 »Æѧ·“Ó¦ŌĄķŌŚæĘŃŠŗĶÉś²śÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®
»Æѧ·“Ó¦ŌĄķŌŚæĘŃŠŗĶÉś²śÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČõĖį»ÆѧŹ½ | HClO | H2CO3 |
| µēĄėĘ½ŗā³£Źż | K=4.7”Į10-8 | K1=4.3”Į10-7£¬K2=5.6”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “óĮ¦Ģį³«æŖ·¢»ÆŹÆČ¼ĮĻ×÷ĪŖÄÜŌ“ | |
| B£® | ŃŠ·¢ŠĀŠĶ“߻ƼĮ£¬ĢįøߏÆÓĶŗĶĆŗÖŠø÷×é·ÖµÄČ¼ÉÕČČ | |
| C£® | »ÆŹÆČ¼ĮĻŹōÓŚæÉŌŁÉśÄÜŌ“£¬²»Ó°Ļģæɳ֊ų·¢Õ¹ | |
| D£® | ČĖĄąÓ¦¾”æÉÄÜæŖ·¢ŠĀÄÜŌ“£¬Č”“ś»ÆŹÆÄÜŌ“ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com