
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |
科目:高中化学 来源:不详 题型:单选题
| A.正极附近SO42-浓度逐渐增大 |
| B.电子通过导线由铜片流向锌片 |
| C.正极反应式为Zn-2e-=Zn2+ |
| D.该原电池工作过程中电解质溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B.放电时正极反应为:FeO42-+4H2O+3e-=Fe(OH)3+5OH- |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①和③ | B.①和④ | C.②和③ | D.②和④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )| A.充电时阳极反应为Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时OH-向阳极移动 |
| C.放电时每转移3 mol e-正极有1 mol K2FeO4被氧化 |
| D.充电时,电源的正极应与电池的Zn(OH)2极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg·L-1 | 9 360 | 83 | 200 | 1 100 | 16 000 | 1 200 | 118 |


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在熔融电解质中,O2-由负极移向正极 |
| B.通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH- |
| C.通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-=4CO2+5H2O |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体为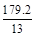 L L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
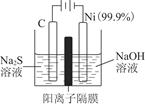

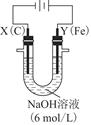
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
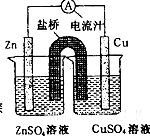
| A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| B.原电池工作时,Zn电极流出电子,发生氧化反应 |
| C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深 |
| D.盐桥中阳离子流向CuSO4溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com