
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg  3Fe+4MgS
3Fe+4MgS
装置如图所示。下列说法不正确的是
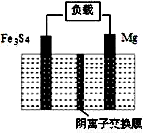
A.放电时,镁电极为负极
B.放电时,正极的电极反应式为Fe3S4+8e-==3Fe+4S2-
C.充电时,阴极的电极反应式为MgS +2e-== Mg+S2-
D.充电时,S2-从阴离子交换膜左侧向右侧迁移
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末文科化学A卷(解析版) 题型:选择题
在一定条件下,反应A2(g)+B2(g)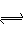 2AB(g),达到反应限度的标志是( )
2AB(g),达到反应限度的标志是( )
A.容器内气体的总压强不随时间的变化而变化
B.单位时间 内有nmolA2生成,同时就有nmolB2生成
内有nmolA2生成,同时就有nmolB2生成
C.单位时间内有nmolA2生成,同时就有2nmolAB生成
D.单位时间内有nmolB2发生反应,同时就有2nmolAB生成
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末理科化学A卷(解析版) 题型:选择题
下列关于苯的叙述正确的是( )
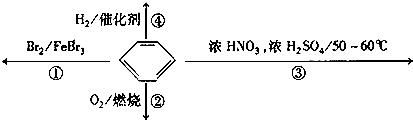
A. 反应①为取代反应,有机产物的密度比水小
B. 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④1mol苯最多与3molH2发生加成反应,是因为苯分子含有三个碳酸双键
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下热身考理综化学试卷(解析版) 题型:选择题
下列操作或装置能达到实验目的的是
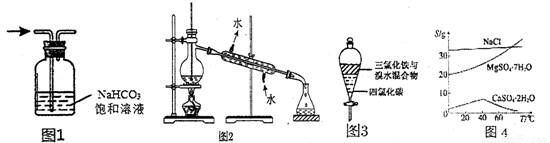
A. 用图1除去氯气中的HCl气体
B. 用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物
C. 用图3所示装置可以萃取,充分振荡后静置,下层溶液为橙红色,上层为无色
D. 根据图4的溶解度变化可知,在较低温度下容易分离MgSO4·7H2O和CaSO4·2H2O
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下模拟考试理综化学试卷(解析版) 题型:实验题
氯化锶晶体在工业上常用作铝的缓蚀剂。工业上一般用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体(SrCl2·6H2O)的过程为:
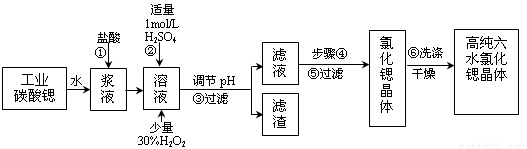
已知:Ⅰ.SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
Ⅱ. 有关氢氧化物开始沉淀和完全沉淀的pH如下表:
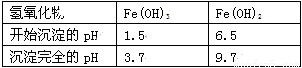
(1)操作①在实际工业生产中常常把碳酸锶粉碎并加以搅拌,其目的是 。碳酸锶与盐酸反应的化学方程式为 。
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为__________。能否用新制氯水代替双氧水 (填“能”或“否”)。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至 ;宜用的试剂为 。
A.1.5 B.4 C.9.7
D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体 G.氧化锶粉末
(4)操作③中所得滤渣的主要成分是 (填化学式)。
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是 。
(6)步骤⑥中,洗涤氯化锶晶体最好选用 。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:填空题
酸牛奶中含有乳酸。它可由乙烯来合成,方法如下:

(1)乳酸自身在不同条件下可形成不同的酯,写出下列结构简式:两分子成环酯 、两分子成链状酯 。
(2)写出下列转化的化学方程式:
A的生成 。
CH3CHO的生成 。
C的生成 。
(3)A→B的反应类型为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:选择题
1,4-二氧六环 是一种常见溶剂,它可以通过下列方法制得:
是一种常见溶剂,它可以通过下列方法制得:

则烃类A可能是
A.1-丁烯 B.1,3-丁二烯 C.乙炔 D.乙烯
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:选择题
40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如图所示.下列说法不正确的是( )
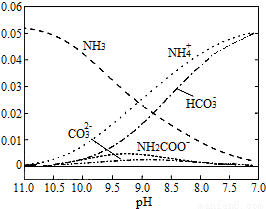
A.在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-)
B.不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)
C.随着CO2的通入,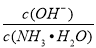 不断增大
不断增大
D.在溶液pH不断降低的过程中,有含NH2COO-的中间产物生成
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下期中化学试卷(解析版) 题型:推断题
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的单质和它的一种氧化物是工业生产上常用的还原剂。B的最外层电子数是次外层的3倍;0.1molC的单质能从酸溶液中置换出2.24L标准状况下的氢气;又知B、C、D所形成的简单离子的电子层结构相同,B和E是同主族的元素。请回答下列问题:
(1)请依次写出A、C、E三种元素的元素符号: 、 、 。
(2)请写出A的最高价氧化物的电子式 ;E的单质在空气中燃烧所生成物质的化学式 。
(3)A元素可以形成多种同素异形体,其中硬度最大,不导电的是 (填物质名称);熔点高,可以导电的是 (填物质名称)。
(4)请写出C的单质与A、B形成的化合物反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com