
| A、装修新房季节最好选择夏季 |
| B、适度开窗通风,充分地进行内外空气对流 |
| C、用高浓度的甲醛对室内环境消毒 |
| D、在各个房间内均匀的放置适量的吊兰、芦荟等鲜花 |


科目:高中化学 来源: 题型:
| A、两种溶液各取少许,分别滴入酚酞试液,显红色的是碳酸钠溶液 |
| B、两种溶液各取少许,分别滴加澄清的石灰水,有沉淀生成的是碳酸钠溶液 |
| C、两种溶液各取少许,分别加热,能产生使澄清的石灰水变浑浊气体的是碳酸氢钠溶液 |
| D、任取一种溶液少许,滴加氯化钡溶液,若有浑浊产生的是碳酸钠溶液,否则是碳酸氢钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
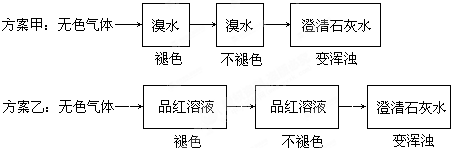
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m1=m2 |
| B、混合物A中CaCO3和KHCO3质量比一定为1:1 |
| C、25m1=21m2 |
| D、混合物B中MgCO3和NaHCO3质量比可为任意比 |
查看答案和解析>>
科目:高中化学 来源: 题型:
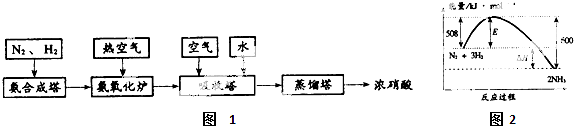

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
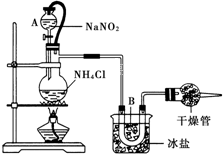 实验室常用饱和NaNO2与NH4Cl溶液反应制取纯净氮气,如图.反应式为:NaNO2+NH4Cl═NaCl+N2↑+2H2O;反应放热.试回答:
实验室常用饱和NaNO2与NH4Cl溶液反应制取纯净氮气,如图.反应式为:NaNO2+NH4Cl═NaCl+N2↑+2H2O;反应放热.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.5mol?L-1 |
| B、2mol?L-1 |
| C、2.5mol?L-1 |
| D、3mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com