
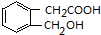
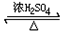
 +H2O(有机物须用结构简式表示)
+H2O(有机物须用结构简式表示)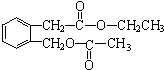 ;反应④的反应类型是消去反应.
;反应④的反应类型是消去反应. .
. .
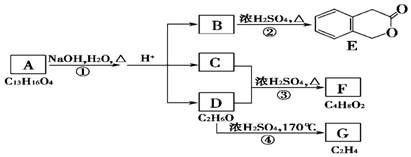
. 分析 A、B、C、D、E、F、G均为有机化合物,A能发生水解反应,则A为酯,B发生酯化反应生成E,根据E结构简式知,B为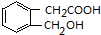 ;D发生消去反应生成乙烯,G为CH2=CH2、D为CH3CH2OH,C和D发生酯化反应生成F,根据A和BD分子式知,C结构简式为CH2COOH,则A结构简式为
;D发生消去反应生成乙烯,G为CH2=CH2、D为CH3CH2OH,C和D发生酯化反应生成F,根据A和BD分子式知,C结构简式为CH2COOH,则A结构简式为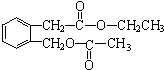 ,据此分析解答.
,据此分析解答.
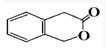
解答 解:(1)B在浓硫酸加热条件下生成E,由E的结构可知,B发生酯化反应生成E,故B为 .D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,名称为乙酸,
.D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,名称为乙酸,
故答案为:乙酸;
(2)B为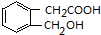 ,B发生酯化反应生成E,反应②的化学方程式是:
,B发生酯化反应生成E,反应②的化学方程式是: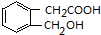
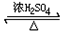
 +H2O,
+H2O,
故答案为: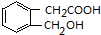
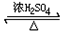
 +H2O;
+H2O;
(3)反应③是CH3COOH与CH3CH2OH发生酯化反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH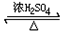 CH3COOC2H5+H2O,所以F为CH3COOC2H5,
CH3COOC2H5+H2O,所以F为CH3COOC2H5,
F的分子式为C4H8O2,A能发生水解反应生成物酸化后的BCD分别为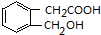 、CH2COOH、D为CH3CH2OH,所以A结构简式为
、CH2COOH、D为CH3CH2OH,所以A结构简式为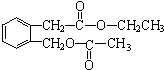 ,反应④为乙醇的消去反应,生成乙烯,反应为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
,反应④为乙醇的消去反应,生成乙烯,反应为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:C4H8O2;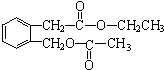 ;消去反应;
;消去反应;
(4)B为 ,B的同分异构体:i)含有邻二取代苯环结构,说明含有两个取代基且处于邻位,ii)与B有相同官能团说明含有醇羟基和羧基,iii)不与FeCl3溶液发生显色反应,说明不含酚羟基,所以其同分异构体为
,B的同分异构体:i)含有邻二取代苯环结构,说明含有两个取代基且处于邻位,ii)与B有相同官能团说明含有醇羟基和羧基,iii)不与FeCl3溶液发生显色反应,说明不含酚羟基,所以其同分异构体为 ,有3种同分异构体,
,有3种同分异构体,
故答案为:3; ;
;
(5)G是乙烯,乙烯能发生加聚反应生成聚乙烯,反应方程式为:nCH2=CH2$\stackrel{催化剂}{→}$ ,
,
故答案为:nCH2=CH2$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物的推断,为高频考点,侧重考查学生分析推断及知识综合运用能力,难点是同分异构体的推断,注意根据题给信息确定含有的官能团及其结构,从而确定该有机物的结构简式,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
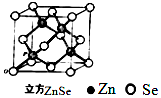 硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.
硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
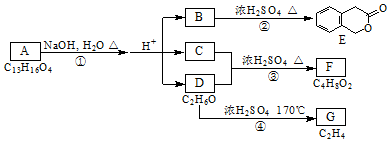
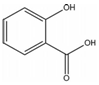 ,其名称为:邻羟基苯甲酸
,其名称为:邻羟基苯甲酸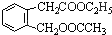 ④反应的反应类型是消去反应
④反应的反应类型是消去反应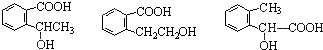 任意一个
任意一个 或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.
或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2既能溶于NaOH溶液又能溶于氢氟酸,说明SiO2是两性氧化物 | |
| B. | 将Cu片置于浓H2SO4中,无明显现象,说明Cu在冷的浓硫酸中被钝化 | |
| C. | “雷雨发庄稼”的实质是自然固氮 | |
| D. | 自来水厂可用明矾对水进行杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同 | |
| B. | 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度 | |
| C. | 用加热的方法可以除去KCl溶液中的Fe3+ | |
| D. | 锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
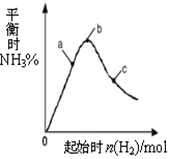 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com