
 CaO2+2HCl.
CaO2+2HCl.| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| CaO2平均生成速率(×10-3mol.s-1) | 7.5 | 8.2 | 9.4 | 8.0 | 7.1 | 6.7 | 5.5 |
 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量.
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量. 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1.| 时间/s | n(CaO2)/mol | n(CaO)/mol | n(O2)/mol |
| 0 | 2 | 0 | 0 |
| 1 | 1.4 | 0.6 | 0.3 |
| 2 | 1 | 1 | 0.5 |
| 3 | 1 | 1 | 0.5 |
分析 I.(1)①在低温下,往过氧化氢浓溶液中投入无水氯化钙发生复分解反应生成CaO2与HCl;
②为控制低温,最好将反应器放置在冰水浴中;
③40℃之前,温度升高,速率加快;40℃之后,温度继续升高,双氧水分解;
(2)NH3•H2O结合反应生成HCl,使平衡向正方向移动;
II.(3)由标准生成热可得热化学方程式:①Ca(s)+O2(g)=CaO2(s)△H=a kJ•mol-1,
②Ca(s)+$\frac{1}{2}$O2(g)=CaO(s)△H=b kJ•mol-1,
根据盖斯定律,(②-①)×2可得:2CaO2(s)  2CaO(s)+O2(g);
2CaO(s)+O2(g);
(4)发生反应:2CaO2(s)  2CaO(s)+O2(g),2s、3s时,同一组分的物质的量不变,说明2s时反应得到平衡,平衡常数K=c(O2);
2CaO(s)+O2(g),2s、3s时,同一组分的物质的量不变,说明2s时反应得到平衡,平衡常数K=c(O2);
(5)温度不变,该反应的平衡常数K=c(CO2)不变;
(6)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡.
解答 解:I.(1)①在低温下,往过氧化氢浓溶液中投入无水氯化钙发生复分解反应生成CaO2与HCl,反应方程式为:H2O2+CaCl2  CaO2+2HCl,
CaO2+2HCl,
故答案为:H2O2+CaCl2  CaO2+2HCl;
CaO2+2HCl;
②为控制低温,最好将反应器放置在冰水浴中,
故答案为:冰水浴;
③40℃之前,温度升高,速率加快;40℃之后,温度继续升高,双氧水分解,浓度下降,反应速率减慢,
故答案为:40℃之前,温度升高,速率加快;40℃之后,温度继续升高,双氧水分解,浓度下降,反应速率减慢;
(2)NH3•H2O结合HCl,使反应H2O2+CaCl2 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量,
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量,
故答案为:NH3•H2O结合HCl,使反应H2O2+CaCl2 CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量;
CaO2+2HCl平衡向正方向移动,提高过氧化钙的产量;
II.(3)由标准生成热可得热化学方程式:①Ca(s)+O2(g)=CaO2(s)△H=a kJ•mol-1,
②Ca(s)+$\frac{1}{2}$O2(g)=CaO(s)△H=b kJ•mol-1,
根据盖斯定律,(②-①)×2可得:2CaO2(s) 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1,
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1,
故答案为:2CaO2(s) 2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1;
2CaO(s)+O2(g)△H=2(b-a)kJ•mol-1;
(4)发生反应:2CaO2(s)  2CaO(s)+O2(g),2s、3s时,同一组分的物质的量不变,说明2s时反应得到平衡,平衡常数K=c(O2)=$\frac{0.5mol}{2L}$=0.25mol/L,
2CaO(s)+O2(g),2s、3s时,同一组分的物质的量不变,说明2s时反应得到平衡,平衡常数K=c(O2)=$\frac{0.5mol}{2L}$=0.25mol/L,
故答案为:0.25mol/L;
(5)温度不变,该反应的平衡常数K=c(CO2)=0.25mol/L不变,故氧气的浓度不变,
故答案为:不变;温度不变,该反应的平衡常数K=c(CO2)=0.25mol/L不变;
(6)a.反应体系中只有氧气为气体,恒温恒容条件下,随反应进行容器内气体密度增大,气体的密度保持不变,说明反应到达平衡,但若在恒温恒压下条件下,氧气的密度不变,故a错误;
b.反应有氧气生成,随反应进行固体质量减小,而固体质量不再改变,说明反应到达平衡,故b正确;
c.可能反应到达平衡时只能反应速率相等,不再变化,故c正确;
d.可能反应到达平衡时只能反应速率相等,不再变化,故d正确.
故选:a.
点评 本题以过氧化钙的制备为载体,考查对制备原理的分析与评价、化学平衡计算与影响因素、平衡状态判断、热化学方程式书写、陌生方程式书写等,是对学生综合能力的考查.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:解答题
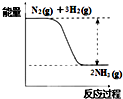 在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.
在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
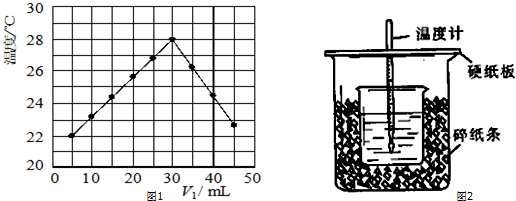
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
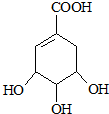
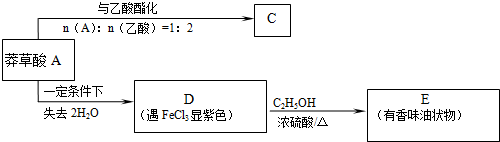
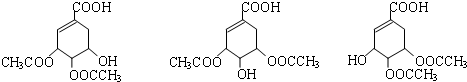 .
.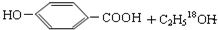 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$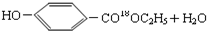 ②E与足量的NaOH溶液反应
②E与足量的NaOH溶液反应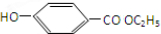 +2NaOH→
+2NaOH→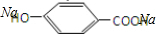 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
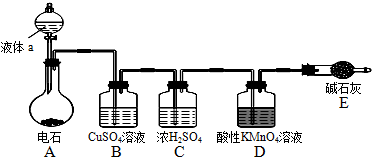
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
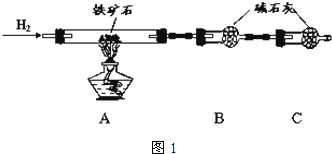 铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应).某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究.
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应).某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究.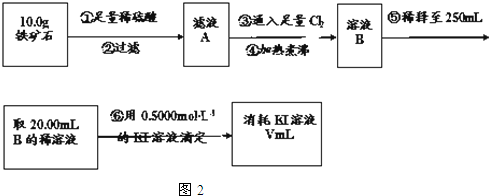
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com