
(8分)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_______ __ ___。
(2)若溶液M由10 mL 2 mol·L-1 NaHA溶液与2 mol·L-1 NaOH溶液等体积混合而得,
则溶液M的pH_ __7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_ _ __。
(3)若溶液M有下列三种情况:
①0.01 mol·L-1的H2A溶液
②0.01 mol·L-1的NaHA溶液
③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,
则三种情况的溶液中H2A分子浓度最大的为___ ___;pH由大到小的顺序为__ ____。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为___ _____(填“大于、等于、小于”或“均有可能”)。
(8分)
(1)H2A H++HA- ,HA-
H++HA- ,HA- H++A2-(2分)
H++A2-(2分)
(2)>(1分),c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) (2分)
(3)③(1分), ②>③>① (1分),
(4)均有可能(1分)
【解析】
试题分析:(1)因为该溶液中存在H2A分子、HA-、A2-,说明该酸是弱酸,所以电离方程式为H2A H++HA- ,HA-
H++HA- ,HA- H++A2-;
H++A2-;
(2)10 mL 2 mol·L-1 NaHA溶液与2 mol·L-1 NaOH溶液等体积混合,生成Na2A,因为A2-的水解会使溶液呈碱性,A2-+H2O HA-+OH-,所以混合后的溶液pH>7,溶液存在的离子是Na+、HA-、A2-、H+、OH-,不水解的离子大于水解离子的浓度,所以离子浓度的大小关系是c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);
HA-+OH-,所以混合后的溶液pH>7,溶液存在的离子是Na+、HA-、A2-、H+、OH-,不水解的离子大于水解离子的浓度,所以离子浓度的大小关系是c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);
(3)①②相比,②中的HA-水解才得到H2A,所以①中的H2A浓度大;③混合后的溶液是0.01 mol·L-1的H2A与0.01 mol·L-1的NaHA溶液的混合液,因为NaHA的存在,使H2A的电离受到抑制,所以③中H2A的浓度大于①,则③的溶液中H2A分子浓度最大;①③溶液呈酸性,且③中的H2A的电离受到抑制,所以①溶液的酸性强,pH小;②的溶液呈碱性,所以三种溶液的pH由大到小的顺序是②>③>①;
(4)混合溶液c(H+)/c(OH-)=104,则c(H+)=10-5mol/L,说明混合后的溶液呈酸性,因为H2A为弱酸,pH=3H2A溶液与pH=11的NaOH溶液相比,氢离子浓度与氢氧根离子浓度相等,则酸的浓度大于碱的浓度,等体积或酸的体积大或者酸的体积小,但酸的物质的量多时,混合后的溶液都会呈酸性,所以不能确定V1与V2的大小关系。
考点:考查酸碱混合的计算,溶液中离子浓度的比较,溶液pH的判断


科目:高中化学 来源:2014-2015学年福建省宁德市五校高二上学期期中化学试卷(解析版) 题型:选择题
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-===ZnO+H2O; Ag2O+H2O+2e-===2Ag+2OH-,下列说法正确的是
A.Zn为正极,Ag2O为负极
B.Ag2O发生还原反应
C.原电池工作时,正极区溶液pH值减小
D.原电池工作时,负极区溶液pH值增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:选择题
下列有关溶液中微粒的物质的量浓度的关系,正确的是
A.0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合的溶液:c(Cl-)>c(Na+)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c( )
)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(H2A)=c(H+)+2c(A2-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三上学期期中理综化学试卷(解析版) 题型:填空题
(16分)已知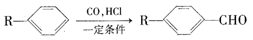
为合成某种液晶材料的中间体M,有人提出如下不同的合成路径:
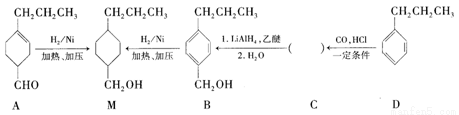
(1)常温下,下列物质能与A发生反应的有________(填序号)。
a.苯 b.Br2/CCl4 c.乙酸乙酯 d.KMnO4/H+ 溶液
(2)M中官能团的名称是_______,由C→B的反应类型为__________。
(3)由A催化加氢生成M的过程中,可能有中间产物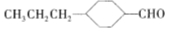 和______(写结构简式)生成。
和______(写结构简式)生成。
(4)检验B中是否含有C可选用的试剂是___________(任写一种名称)。
(5)物质B也可以由C10H13Cl与NaOH水溶液共热生成,C10H13Cl的结构简式为_______。
(6)C的一种同分异构体E具有如下特点:
a.分子中含—OCH2CH3 b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三上学期期中理综化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中能大量共存的是
A.在无色溶液中: Na+、Cu2+、NO3- 、MnO4-
B.在含有HCO3-的溶液中:H+、K+、SO42-、Cl-
C.PH=1的溶液中:Na+、 K+、AlO2-、SO42-
D.常温下,水电离的c(H+)=10-12mol·L-1的溶液中:K+、Ba2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省等四校高三上学期期中联考化学试卷(解析版) 题型:选择题
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH )> c(SO
)> c(SO )>c(Fe2+)>c(H+)
)>c(Fe2+)>c(H+)
B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
C.0.1 mol·L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO )
)
D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c(CH3COO-)>c (Na+)>c(H+)> c (OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省等四校高三上学期期中联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法中不正确的是
A.标准状况下,1.12L的H2O所含的原子数大于0.15NA
B.常温常压下,1mol甲基(—14C1H3)所含有的中子数和电子数分别为8NA和9NA
C.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA
D.在1L0.1mol·L-1碳酸钠溶液中,阴离子总数大于0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3,若将X通入澄清石灰水中,无沉淀产生,则有关气体X的成分的下列说法正确的是
①一定含有HBr,可能含有CO2 ②一定不含CO2 ③一定不含NH3、Cl2 ④可能含有Cl2、CO2
A.①和③ B.只有③ C.只有① D.②和③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期第二次模考试化学试卷(解析版) 题型:选择题
下列有关金属的说法中不正确的是
A.纯铁比生铁的抗腐蚀性强
B.青铜、不锈钢、硬铝都是合金
C.铝在空气中耐腐蚀,所以铝是不活泼金属
D.人体缺钙会引起骨质疏松症,缺铁会引起贫血
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com